Автор: Теодора К. Пискова
2015-та година остава в историята на научните среди с новия революционен метод за геномно редактиране – технологията CRISPR/Cas9. Сензационното откритие представлява изключително прецизен, ефикасен, бърз и евтин начин за манипулиране на ДНК, който обещава да ускори геномните изследвания и да предложи лек срещу рак и срещу редица наследствени болести. Статията има за цел да запознае читателя с метода и неговите предимства, с областите на приложение, както и с етичните предизвикателства, пред които това откритие ни поставя.

В декемврийското си издание за 2015 г. сп. Science обяви CRISPR/Cas9 за научно откритие на годината.
CRISPR/Cas9
CRISPR („Clustered regularly-interspaced short palindromic repeats”) са сегменти от прокариотна ДНК, които съдържат множество повторения на къси части от гени. Те са описани за пръв път в края на 80-те години, а в периода 2005-2007 година се изясни и тяхната роля: заедно с Cas („CRISPR-associated protein”) – ендонуклеаза, т.е. ензим, който може да разрязва ДНК, те образуват бактериална система за придобит имунен отговор.
През 2012 екип от учени, включително Денифър Даунда и Емануеле Шарпентие, които независимо една от друга изследват ендонуклеазата Cas9, успяват да я приложат, заедно със синтетична единична водеща РНК (single-guide RNA), за откриване и срязване на човешка ДНК в култура на точно определено място. Оттогава технологията се изследва с цел приложение в геномното редактиране, като през 2015 е вече значително оптимизирана.
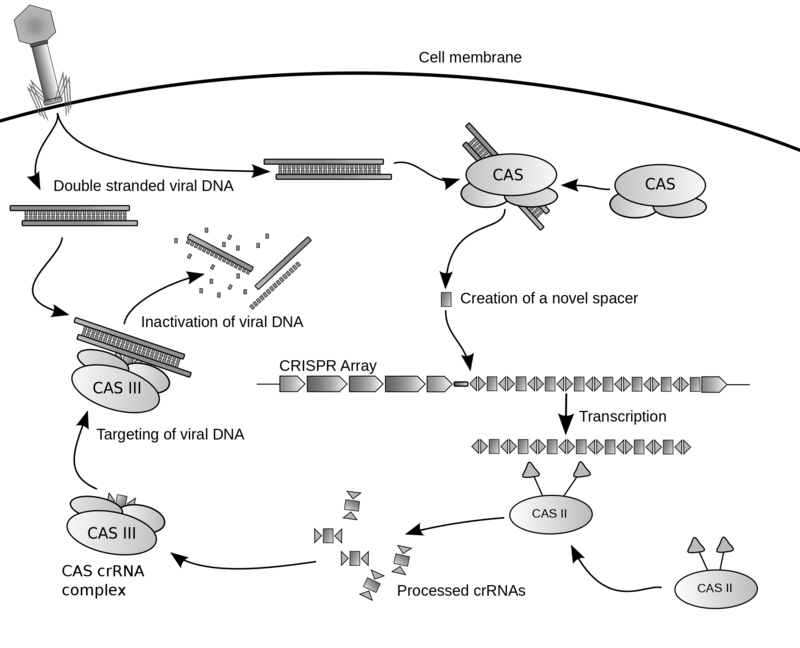
Когато вирус нападне бактерия, тя е способна да копира част от гените му и да ги интегрира в собствения си геном като своеобразна памет – CRISPR. Съхранените повторения биват използвани за синтез на РНК, която се свързва с Cas – протеин и служи за сканиране и разпознаване на вирусната ДНК. След разпознаването й Cas като нуклеаза я разрязва и възпрепятства възпроизводството на вируса.
Заради прецизността си методът често е обозначаван като „молекулярна ножица”. Два компонента играят ключова роля: единична водеща РНК (single guide RNA, sgRNA, gRNA) и ендонуклеазата Cas9. Водещата РНК разполага с регион за свързване с Cas9 и с област, която съответства на целевата част от клетъчния геном. Така тя образува комплекс с Cas9, разпознава мястото за срязване и „завежда” нуклеазата до целта. Функцията на Cas9 е самото разрязване на ДНК.
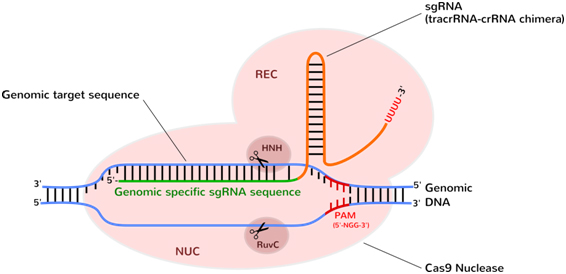
Комплексът от Cas9 и sgRNA. Участък (в оранжево) от sgRNA се свързва с Cas9 (бледорозово). Сегмент от sgRNA (в зелено) свързва комплекса с геномната ДНК. Ножиците обозначават местата, където Cas9 срязва ДНК.
Гени за sgRNA и Cas9 биват доставени на клетата и тя сама произвежда необходимите за процедурата компоненти. Образува се Cas9/sgRNA-комплексът. Целевата част от генома бива разпозната чрез sgRNA и прецизно срязана от ендонуклеазата Cas9.
Клетката разпознава срязаната клетъчна ДНК като повредена и стартира собствения си механизъм за поправка на ДНК. Съществуват два варианта за поправянето:
- Non-Homologous End Joining (нехомоложно събиране/слепване на краищата) е естественият процес, който се случва при липса на външна намеса. Целостта на разрязаната ДНК бива възстановена. Получават се случайни точкови мутации, делеции и/или инсерции – промяна, изтриване и/или вмъкване на нуклеотиди в ДНК. С помощта на технологията може да се постигне и „изключване на ген”, което служи за изследване на функциите му.
- Homology Directed Repair (хомоложно насочено поправяне) се наблюдава при наличие на шаблон за поправка. Той представлява къса ДНК-последователност с краища, еднакви с двете страни на разреза. Използва се за вмъкване на специфични мутации, инсерции и делеции и за „изключване”, „включване” и маркиране на гени.
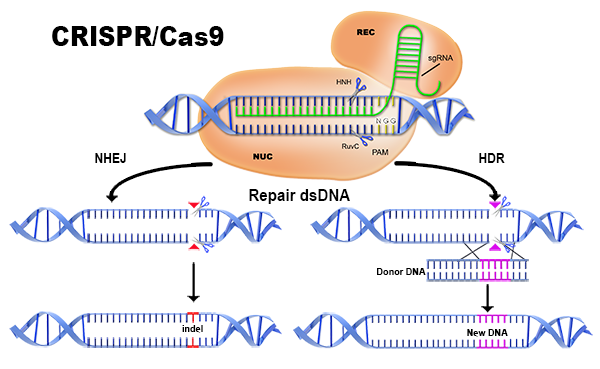
Методи за поправка на срязаната ДНК: Non-Homologous End Joining(отляво) с възникващите точкови мутации(червено) и Homology Directed Repair(отдясно) с шаблон(Donor DNA) и желаната мутация.
Предимства и приложения
Учените от години са способни да манипулират клетъчния геном. Методи, включващи нуклеазите „цинкови пръсти” (zinc finger nucleases) и така наречените TALENs (transcription activator-like effector nucleases) представляват голям напредък в геномното редактиране през миналото десетилетие. В сравнение с технологията CRISPR/Cas9, те са непрецизни, бавни, сложни за произвеждане и скъпи. Огромно предимство на новия метод е и възможността за редактиране на повече от един ген едновременно.
CRISPR/Cas9 е приложен успешно за редактиране на гени в клетки на редица организми: човек, дрожди, риба „зебра”, винена мушица, растения и мишка. Учените виждат в технологията потенциал за приложение в различни научни области, в генното изследване, генното инженерство и генната терапия, регенеративната медицина, в изследването на болести и разработването на медикаменти.
Морален аспект
След представянето на многообещаващия метод, няколко лаборатории в САЩ, Обединеното Кралство и Китай заявяват плановете да използват CRISPR/Cas9 върху човешки ембриони. В отговор, редица учени, сред които и Дженифър Даунда, настояват за световен мораториум върху приложението на метода върху репродуктивни клетки.
През април 2015 година китайски учени използват CRISPR/Cas9 за корекция на летална мутация в човешки ембриони. Изследователската общност, включително и списанията Nature и Science заклеймяват проекта от етични съображения. Експериментите завършват с успешно отстраняване на мутиралия ген, но и с други непланирани промени. Изводът: технологията не е готова за клинично приложение в репродуктивната медицина.
В началото на декември 2015 във Вашингтон се провежда Международна среща на високо ниво относно генно редактиране на човешки клетки (International Summit on Human Gene Editing). Членове на национални изследователски академии от САЩ, Обединеното Кралство, Германия и Китай дискутират етиката на редактирането на човешката зародишна линия. Според становището, с което учените излизат след мероприятието, може да се продължи с основни и клинични изследвания, които не нарушават общоприетите законни и етични норми. Прави се разграничение между прилагането на генно редактиране върху соматични клетки, където направените промени се отразяват само на отделния индивид, от това върху репродуктивни клетки, където промененият геном бива наследен от следващите поколения. В първия случай ограниченията са сравнително малко, а учените считат, че изследванията на гамети (полови клетки – яйцеклетки и сперматозоиди) и ембриони все още са рисковани.

Все пак: През февруари 2016 британски учени получават разрешение за генетично модифициране на човешки ембриони. Ембрионите трябва да бъдат разрушавани в рамките на седмица след интервенцията.
Библиография:
Applied biological materials – abm. CRISPR Cas9 – A Brief Introduction. www.youtube.com, 21-26.03.2016, https://www.youtube.com/watch?v=1aJxXWkE3Ek
Zhang, Feng; Wen, Yan; Guo, Xiong. CRISPR/Cas9 for genome editing: progress, implications and challenges. // Human Molecular Genetics, 2014, Vol. 23, Issue R1. oxfordjournals.org, 23-26.03.2016, http://hmg.oxfordjournals.org/content/23/R1/R40.long
Wikipedia. CRISPR. wikipedia.org, 21-26.03.2016, https://en.wikipedia.org/wiki/CRISPR
Snyder, Bill. New technique accelerates genome editing process. news.vanderbilt.edu, 25.03.2016, http://news.vanderbilt.edu/2014/08/new-technique-accelerates-genome-editing-process
International Summit On Human Gene Editing. On Human Gene Editing:International Summit Statement. www8.nationalacademies.org, 26.03.2016, http://www8.nationalacademies.org/onpinews/newsitem.aspx?RecordID=12032015a


