Фотодинамичната терапия на някои видове рак разкри удивителен страничен ефект – лекуваните пациенти започват да виждат по-добре през нощта. Изследователите успяха да разгадаят механизмите на тази изненадваща зрителна острота благодарение на молекулярната симулация.

Сн.1. Credit: Engin Akyurt, pexels.com
Това е озадачаващ страничен ефект от фотодинамичната терапия – лечение, при което се прилага фоточувствително лекарство, използвано и при лечението на някои ракови заболявания такива като рак на кожата, на хранопровода или бронхите, а така също и на някои бактериални инфекции. „От началото на 2000-те години започнаха да се появяват статии, в които се съобщава, че пациентите, лекувани с хлорин е6, виждат силуети и контури в тъмното и са доста смутени от случващото се“, казва Антонио Монари, химик и специалист по молекулярна симулация.
Принципът на тези фототерапевтични лечения е добре известен – лекарството се активира от лазерен лъч – инфрачервено лъчение, проникващо на малка дълбочина в тъканите, което унищожава туморните клетки чрез производството на синглетен кислород. Но каква е връзката на хлорина e6, използван за елиминиране на туморните клетки, със зрението? Това се опитали да разберат Антонио Монари и неговите колеги чрез използването на молекулярна симулация, която позволява да се имитират биохимични реакции изцяло на компютър.
За да можем да виждаме, светлината се събира от набор от рецептори, разположени в ретината. Родопсинът, светлочувствителен рецепторен протеин, играе съществена роля в този процес, като абсорбира видимата светлина благодарение на активния алдехид ретинал, производен на витамин А. „При получаването на светлина, ретиналът променя химическата си структура, отделяйки се от протеина, което позволява преобразуването на светлинния сигнал в електрически, който вече може да се интерпретира от зрителния кортекс “, обяснява Антонио Монари. В условия на слаба осветеност, особено през нощта, преобладаващото светлинно излъчване вече не е във видимия спектър, а в инфрачервения, към който ретиналът не е чувствителен. Ето защо за разлика от много други животински видове, ние не можем да виждаме в тъмното.
„Благодарение на експериментите, проведени от биолозите през последните години, ние знаем, че при инфрачервено лъчение химическата структура на ретинала се променя след инжектиране на хлорин – говорим за изомеризация – по същия начин, както когато получава видима светлина. Това обяснява наблюдаваното увеличение на зрителната острота през нощта”, допълва Монари. „Въпреки това, досега нямахме представа как точно родопсинът и неговата ретинална група си взаимодействат с хлорина. Благодарение на молекулярната симулация успешно изяснихме този механизъм. „
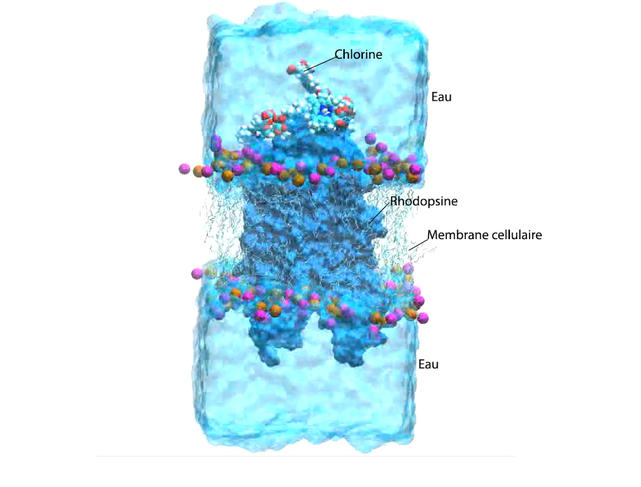
Фиг.2. Молекулярната симулация показваща химичното взаимодействие между молекулата хлорин и родопсина. Credit: LPCT/Univ de Lorraine – CNRS
Този метод, използван в биологията в последните десетина години, позволява благодарение на алгоритмите, интегриращи законите на Нютоновата физика и на квантовата физика, и двете на атомно ниво, да се имитира функционирането на една биологична система във времето.
Движението на всеки от атомите се моделира според привличането му или отблъскването му от съседните атоми, както и разкъсването или напротив – създаването на нови химически връзки.
„За целите на нашата симулация събрахме виртуален протеин родопсин, вкаран в липидната му мембрана, няколко молекули хлорин е6 и вода, тоест десетки хиляди атоми“, казва Антонио Монари. „Нашите суперкомпютри работиха в продължение на няколко месеца, извършвайки милиони изчисления, преди да сме в състояние да симулираме цялата биохимична реакция, предизвикана от инфрачервеното лъчение. Беше ни необходимо цялото това време, за да симулираме това явление в цялата му сложност, което иначе се случва само за няколкостотин наносекунди … „
Поглъщайки инфрачервеното лъчение, хлоринът е6 взаимодейства с кислорода, присъстващ в тъканите на окото, и го превръща в синглетен кислород, както е наблюдавано при раковите лезии. Антонио Монари и неговите колеги от университетите в Алкала де Енарес и Валенсия в Испания, и този на Нанкай в Китай успяха да покажат, че този синглетен кислород прониква в молекулата на родопсина и се натрупва до ретинала, причинявайки неговата изомеризация. „Тъй като имаме слабо инфрачервено лъчение – нищо общо със силата на лазерния лъч, използван във фототерапията – няма производство на достатъчно синглетен кислород, който да предизвика унищожаването на клетките на окото” , успокоява Антонио Монари. „Но има достатъчно, за да може нощното виждане да бъде леко подобрено. „
Разбирането на този механизъм може в крайна сметка да неутрализира този страничен ефект при пациенти, лекувани с фотодинамична терапия, и отваря интересни перспективи за разработване на алтернативни методи за лечение на слепота или свръхчувствителност при светлина. „А защо и да не си представим да възпроизведем този механизъм като го усъвършенстваме, така че да можем да виждаме през нощта, но този път вече умишлено“, завършва Монари.
Резултатът от проучването показва какви могат да бъдат ползите от прилагането на молекулярната симулация за по-доброто разбиране на биологичните системи. „Ние сме едва в началото, тъй като е трудно да се симулират системи, включващи твърде големи молекули. Но молекулярната симулация вече се използва, за да хвърли повече светлина върху фундаментални механизми и позволява да се направи подбор на потенциални терапевтични молекули чрез имитиране на взаимодействието им за предвидената цел“, заключава изследователят.
Превод: Елена Страхилова
Източник: CNRS


