Николай Адамов – Факултет по химия и фармация, Софийски университет, София, България
Теодора Данева – Институт по Биология и Имунология на Размножаването – БАН, София, България
Резюме
Технологията CRISPR/Cas9 е фундаментално и много важно откритие за съвременната биология, което ние разглеждаме просто като начин за редактиране на генома. Той се крие във факта, че огромен брой бактерии носят в генома си ефективна система на адаптационен имунитет срещу потенциална вирусна инвазия. Основата на тази система са специални геномни региони – къси палиндромни клъстерни повторения или CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats).
В крайна сметка технологията CRISPR/Cas9 може да промени гледната точка на човечеството към много различни наследствени заболявания. Ако по-рано те са били или напълно нелечими, или са разрешавали палиативно симптоматично лечение, вече би било възможно да се лекуват чрез манипулиране на отделни гени, тоест да се елиминира самата причина за съответното заболяване. Едновременно с появата на технологията за редактиране на генома, се появява възможността за нейното „подобряване“ по различни начини. За сега доста прости (от гледна точка на механизма за наследяване) болести и не само мутантни гени могат да бъдат потенциално мишени за редактиране, но и много гени, свързани с повишен риск за човешкото здраве. Много допълнителна работа предстои да се извърши в областите манипулиране и заместване на нуклеотиди, преди да може да се реализира пълният терапевтичен потенциал на тези подходи. Също толкова важно е да се вземат предвид всички морални и етични въпроси, свързани с терапиите за редактиране на гени, преди да се приложи какъвто и да е практически подход.
Въведение
Разработени са различни технологии за манипулиране на ДНК, но доскоро те бяха скъпи, трудоемки и отнемаха много време. Откриването на клъстерираните равномерно разположени къси палиндромни повторения (CRISPR), механизмът на базираната на CRISPR прокариотна адаптивна имунна система (свързана с CRISPR система, Cas) и превръщането й в мощен инструмент за редактиране на ДНК промени напълно науката за манипулацията на гените. Редактирането на генома с CRISPR/Cas9 произлиза от естествения защитен механизъм, използван от бактериите, да се предпазат от инфекция от бактериофаги и подвижни генетични елементи. В природата CRISPR функционира като бактериална адаптивна имунна система, произвеждайки РНК-и комлементарни на чуждите вирусни ДНКи, маркирайки ги за унищожаване. След първоначалния интензивен период на натрупване на данни, CRISPR скоро беше адаптирана за широк спектър от приложения – създавайки сложни животински модели на наследствени заболявания при човека и ракови заболявания; извършване на обследване на целия геном в човешки клетки за определяне на гените, отговарящи на специфични биологични процеси; регулиране на експресията на специфични гени; използвани за генетично модифициране на растения. Тази технология отвори безброй възможности за лесно, евтино и бързо редактиране на човешки гени. Тя буквално има потенциала да промени човешката медицина и здраве. Защо се случи тази внезапна революция и как работи тя?
История и произход
От древни времена човечеството се опитва да управлява живота и хода на еволюцията чрез изкуствен подбор, селектиращ белезите от растения и животни, получени чрез случайни мутации, които са най-полезни и значими. Чрез селективно развъждане селектирахме полезните свойства на растенията и животните. Този процес обаче отнема много време. Ставаме много добри в това, но така и не разбирахме напълно как работи, докато не открихме ДНК. През 20-ти век е открита структурата на ДНК и са открити много възможности за изследване. През 70-те години се правят опити за ускоряване на тези мутации чрез третиране на растителни култури с различни мутагенни фактори като радиация или химикали и скрининг на полезните. През 70-те години учените вмъкват ДНК фрагменти в бактерии, растения и животни, за да ги модифицират за изследвания, медицина, селско стопанство и дори за забавление. Това поставя началото на генното инженерство. Днес ние произвеждаме много вещества чрез генното инженерство като животоспасяващи фактори на съсирването, хормони като инсулин и хормон на растежа, растежни фактори и други. Всички неща, които трябваше да се извличат от органите на животните преди това, сега се произвеждат чрез генно инженерни методи.
По време на своята еволюция бактериите са разработили набор от механизми, за да се предпазят от нашественици като фаги и плазмидни нуклеинови киселини. Съществуват различни прокариотни защитни системи и поне две от тях са насочени директно към инвазивната ДНК: Рестрикционна Модификация (RM) и CRISPR-Cas система. И двете системи са съвместими и действат заедно за повишаване на бактериалната устойчивост към фаги чрез нарязване на съответните им целеви места и за намаляване на заразяванията с фаги.
Идентифицирана е специфична последователност от повтарящи се гени в E. Coli, показваща пет силно хомоложни последователности от 29 нуклеотида, подредени като директни повторения с 32 нуклеотида като интервал [1].
Haloferax Mediterranei е архебактериален организъм с изключителна толерантност към солта и високата концентрация на сол влияе върху начина, по който рестрикционните ензими режат генома на микроба. В изследваните фрагменти на ДНК са открити множество копия на почти перфектна, грубо палиндромна, повтаряща се последователност от 30 базии, разделени с дистанционни елементи от приблизително 36 бази – които не приличат на нито едно семейство повторения, познати в микробите [2].
Името CRISPR – Clustered Regularly Interspaced Short Palindromic Repeats е предложено от Jansen, et al. [3]. През 2005 г. е установено, че повторенията в последователността са геноми от бактериофаги или друг екстрахромозомен произход [4]. През 2007 г. е съобщено, че CRISPR осигурява резистентност срещу вируси в прокариотите [5,6].
Системата CRISPR-Cas е бактериална „имунна система“ срещу бактериофаги. Това е последователност на бактериалния геном, която се състои от повтарящи се къси палиндромни ДНК области с дължина 30-40 нуклеотидни двойки. Те са разделени от участъци от ДНК, наречени „дистанционни елементи“. Тези региони са различни и е установено, че съвпадат идеално с ДНК на бактериофагите, с която бактерията вече се е сблъсквала. С CRISPR последователността са свързани региони на ДНК -Cas гените (CRISPR асоциирани последователности), които кодират CAS информация за протеини. Те са главно хеликази и нуклеази. Поради това CRISPR се нарича „имунна система на бактериите“ [7,8]. През 2009 г. Hale, et al. публикува доказателства, че системата CRISPR-Cas защитава прокариотите от вируси и други потенциални нашественици на геноми чрез уникална система за заглушаване на РНК, която функционира чрез хомоложно зависимо разцепване на нашественици РНК [9]. През 2010 г. Maraffini и Sontheimer са дефинирали механизма на CRISPR саморазпознаване / не-саморазпознаване чрез малки CRISPR РНКи (crRNAs) [10-12]. „Имунната система“ на CRISPR/Cas е изключително адаптирана да разцепва бързо нахлуващата ДНК и има потенциала да генерира по-защитени микробни щамове [13].
Как работи CRISPR
Когато бактериофагът зарази бактериите и инжектира вирусната ДНК в бактериалната клетка, вирусният геном ще принуди клетката да произвежда вирусните протеини и вирусните ензими и след това ще промени цялата клетъчна техника на бактерията. Благодарение на системата CRISPR бактериалната клетка може да предотврати това да се случи втори път. Това е един вид памет за предотвратяване същият бактериофаг да зарази клетката друг път. Системата CRISPR е тристепенен механизъм. Първият е Spacer Acquisition, вторият е обработка на crRNA, а третият е интерференция и деградация на целта. Има три типа CRISPR: тип I, тип II и тип III в зависимост от бактериалната клетка. Когато бактериофагът заразява за първи път бактериална клетка, бактериалната клетка нарязва генома на вируса и взема парче от него и го вмъква в спейсърната ДНК в бактериалния геном. Всеки път, когато вирусът заразява бактериалната клетка, клетката взема част от неговата ДНК и я вкарва в дистанционната ДНК. Ензимите Cas са семейство ензими, които участват в процеса CRISPR. Повечето от Cas ензимите са нуклеази или хеликази. В Spacer Acquisition има двама основни играчи – Cas1 и Cas2. И двата са димери, които образуват комплекс заедно, за да формират Spacer Acquisition. Cas1 може да има нуклеазна и интегразна активност. Те могат да изрежат вирусния геном и да го интегрират в ДНК. Cas2 са ендорибонуклеази и могат главно да режат РНК (някои бактериофаги имат РНК геном).
Има три различни вида обработка на crRNA. При I тип CRISPR повтаря цикли на формата и след това иРНК на messenger ще бъде отрязана от Cas6e или Cas6f. ИРНК ще се нарязва на малки парченца РНК и всяка част съдържа контур и парчето от вирусния геном. Тези малки парченца са crRNA. При обработка от тип II има друг играч, наречен tracrRNA (транс активираща crispr РНК). Това са РНК парчета, които се свързват с crRNA на иРНК. Тогава тРНК ще бъде нарязана от Cas9 и RNase III на парчета, състоящи се от парче вирусен геном, crRNA и trRNA. При тип III Cas6 хомологът ще нарязва иРНК директно върху парче вирусен геном и crRNA.
Третата стъпка също е различна между трите типа CRISPR система. Но като цяло Cas протеинът и crRNA взаимодействат заедно и crRNA ще се интегрира в Cas протеина, за да образува комплекс, съдържащ Cas протеина с парчето crRNA. Разликата е между трите вида. Тип I, когато вирусът заразява втори път бактерии, crRNA ще се свърже с комплементарната верига на вирусния геном. Това свързване ще активира каскада от Cas ензими за нарязване и разграждане на вирусния геном. При тип II основният играч е Cas9. След като вирусната ДНК и crRNA се свържат заедно, самият Cas9 извършва двуверижно накъсване (DSB) във вирусния геном. Cas9 има два домейна, наречени HNH и RuvC (RNase H-подобни ендонуклеазни домейни). Cas9 може да използва тези ендонуклеазни домейни за извършване на двойноверижни накъсвания. При тип I и тип II Interference PAM (Proto Spacer Adjacent Motif) е много важен играч. Когато вирусът заразява бактерии, бактерията отнема парчето от вирусния геном, което е в съседство с PAM последователността. Бактериалната клетка може да разпознае PAM последователността и след това тя взема съседната последователност, за да я добави в спейсърната ДНК и след това, за да образува от нея crRNA и CRISPR комплекс. Защо PAM е важен? Тъй като не само РНК, но и Cas ензимът може да разпознае PAM последователността. PAM увеличава специфичността на разпознаването. PAM е много важен при тип I и тип II, но не и при тип III. При тип III също има Cas ензим, crRNA, но не и PAM и също има каскада от ензими, както при тип I, които унищожават вирусния геном. (Фигура 1)
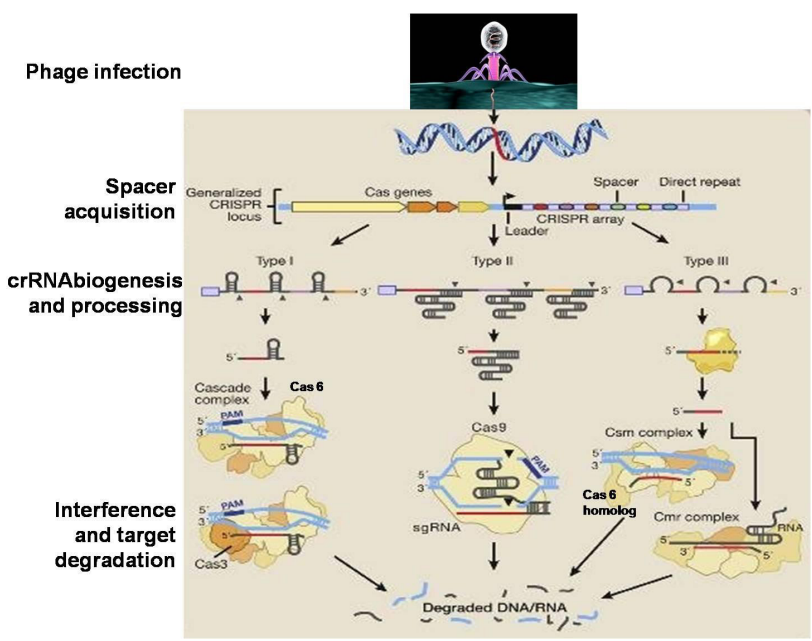
Фигура 1. Система CRISPR/Cas9. Cas9, един от асоциираните протеини, е ендонуклеаза, която реже и двете вериги на ДНК. Cas9 се насочва към целта си от участък от РНК. Тя може да се синтезира като единична верига, наречена синтетична единична РНК (sgRNA); участъкът от РНК, който се свързва с геномната ДНК, е 18–20 нуклеотида. За да се отреже, специфична последователност на ДНК между 2 и 5 нуклеотида (точната последователност зависи от бактериите, които произвеждат Cas9) трябва да лежи в 3 ‘края на водещата РНК: това се нарича съседен мотив на протопространството (PAM) ). Поправянето след изрязването на ДНК може да се осъществи по два пътя: нехомологично свързване на края, обикновено водещо до произволно вмъкване/изтриване на ДНК, или поправка с хомология, когато хомоложно парче ДНК се използва като шаблон за възстановяване. Това е последното, което позволява прецизно редактиране на генома: хомоложният участък от ДНК с необходимата промяна на последователността може да бъде доставен с нуклеазата Cas9 и sgRNA, теоретично позволявайки промени, прецизни като единична двойка бази.
През 2011 г. Babu, et al. съобщават, че освен антивирусен имунитет, поне някои компоненти на системата CRISPR-Cas имат функция и за възстановяване на ДНК [14].
През 2011 г. е публикувано, че активните системи CRISPR/Cas могат да се прехвърлят през отдалечени родове и да осигуряват хетероложна интерференция срещу инвазивни нуклеинови киселини [15]. През 2012 г. Gasiunas, et al. демонстрират, че комплексът Cas9-crRNA на системата Streptococcus thermophilus CRISPR3/Cas9 въвежда in vitro двуверижно прекъсване на специфично място в ДНК, съдържащо последователност, допълваща crRNA ДНК разцепването се извършва от Cas9, който използва две различни активни места, RuvC и HNH, за да генерира специфични за сайта разфасовки на противоположни ДНК вериги. Резултатите показват, че комплексът Cas9-crRNA функционира като РНК-ръководена ендонуклеаза с РНК-насочено разпознаване на целевата последователност и протеин-медиирано разцепване на ДНК. Тези открития проправят пътя за инженериране на универсални програмируеми РНК-ръководени ДНК ендонуклеази [16].
Революцията започва, когато учените разбират, че системата CRISPR е програмируема.
През 2012 г. Дженифър Дудна и Емануела Шарпантие модифицират ензима Cas-9, за да улеснят работата с него. Те създават вариант на Cas-9, който използва едноверижна РНК в комплекса CRISPR-Cas9, който замества crRNA и tracrRNA, която се нарича направляваща РНК (sgRNA). sgRNA съдържа РНК последователност, комплементарна на област на ДНК, която се желае да бъде изрязана. Те са първите, които предполагат, че CRISPR/Cas9 може да се използва за програмируемо редактиране на гени [17], което се счита за едно от най-значимите открития в историята на биологията [18,19]. Оттогава тяхната работа е доразвита от много изследователски групи за приложения, вариращи от фундаментални изследвания на протеини до лечение на заболявания, включително сърповидно-клетъчна анемия, муковисцидоза, болест на Хънтингтън, ХИВ и други.
Приложение
Чрез Cas9 sgRNA е възможно да се правят промени в строго специфичен ген. Основната роля на тази система е да деактивира гените чрез рязане на ДНК молекулата на определено място. Ако Cas9 бъде модифициран, той може да придобие различни функции. Чрез инактивиране на нуклеазната активност и добавяне на други протеини (напр. деаминаза), комплексът Cas9 придобива способността да замества само един нуклеотид. Това прави възможно преобразуването на мутирал ген в здравословната му форма. Друга възможност е пълното инактивиране на неговата нуклеазна активност и добавянето на транскрипционни активатори и по този начин засилване транскрипцията на прицелен ген. Системата CRISPR/Cas9 може да служи за инактивиране/активиране на ген и така може да се използва за изучаването на неговата функция. Можете просто да му дадете копие на ДНК, което искате да модифицирате и да поставите системата в жива клетка. При добавяне на флуоресцентни протеини към Cas9 пространствената структура на генома може да бъде визуализирана, както и маркирането на цялата хромозома. Друго качество на системата е способността да се модифицират живи клетки като соматична и зародишна линия. Освен прецизен, евтин и лесен, CRISPR предлага възможност за редактиране на жизнени клетки, включване и изключване на гени и насочване и изучаване на определени ДНК последователности. Тя също така работи за всеки тип клетки: микроорганизми, растения, животни и хора.
През 2013 г. е извършено прецизно и унаследяемо редактиране чрез CRISPR-Cas на генома на данио [20-23] и на човешки клетки [24-27]. Същата година е ефективно модифициран чрез CRISPR/Cas9 геномът на дрозофила [28,29] и на растения [30,31]. През 2013 г. са публикувани резултати, че системата CRISPR може да се използва като потенциален инструмент за прецизно регулиране на генната експресия в еукариотни клетки [32-36].
Даниото се превърна в популярен модел за изследване на човешките заболявания като невродегенеративни заболявания [37]. Даниото също се е превърнал и в модел за изучаване развитието на сърцето и болестите на сърцето. Прозрачността на ембриона, ограничените му изисквания за активно доставяне на кислород и лекотата при използване на генетични манипулации и химическо излагане го правят мощна алтернатива на използването на гризачи. CRISPR-медиираното генно инженерство и усъвършенстваните образни методи само ще ускорят използването му [38].
Системата CRISPR се превърна в изключително привлекателен подход за изследване на геномните пренареждания като мощна платформа за манипулиране на генома на бозайниците [39-41].
Последният напредък в техниките за редактиране на генома направи възможно модифицирането на всяка желана ДНК последователност чрез използване на програмируеми нуклеази. Β-хемоглобинопатиите, като сърповидно-клетъчна болест и β-таласемия, са причинени от мутации в гена β-глобин и засягат милиони хора по целия свят. Ex vivo генна корекция в получени от пациенти хематопоетични стволови клетки, последвана от автоложна трансплантация, може да се използва за лечение на β-хемоглобинопатии. Тези инструменти за модифициране на геном от следващо поколение са идеалните кандидати за терапевтични приложения, особено за лечение на генетични заболявания като сърповидно-клетъчна анемия (SCA). SCA е наследствено моногенно разстройство, което се причинява от точкова мутация в гена на β-глобин. Постигнат е съществен успех в разработването на поддържащи терапевтични стратегии за SCA, но за съжаление все още липсва дългосрочно универсално лечение. Единственото съществуващо лечение се основава на алогенна трансплантация на стволови клетки от здрави донори. Това лечение обаче е приложимо само за ограничен брой пациенти. Huang и сътр. използвайки CRISPR/Cas9 успешно коригират ендогенната Hbs точкова мутация в индуцирани човешки плурипотентни стволови клетки, изолирани от пациенти със сърповидно-клетъчна анемия и генерират клетки без заболяването за лечение чрез трансплантация обратно на пациентите [42].
Hoban и сътр. демонстрират корекция на сърповидната мутация в получени от пациента CD34 + клетки, използвайки технологията CRISPR/Cas9. Доставката на компонентите CRISPR/Cas9 до CD34 + клетките доведе до над 18% модификация на гена in vitro и корекция на мутацията на сърповидно-клетъчната болест, което довежда до производството на нормален хемоглобин [43].
Dever и сътр. представят CRISPR/Cas9 система за редактиране на гени, която комбинира Cas9 рибонуклеопротеини и адено-асоцииран вирусен вектор за вмъкване на хомоложен донор за постигане на хомоложна рекомбинация при HbS гена в хематопоетични стволови клетки. Те също така предлагат метод за пречистване на популация от хемопоетични стволови и прогениторни клетки с повече от 90% целенасочена интеграция и ефективна корекция на Glu6Val мутацията и експресиране на РНК за нормален β-глобин (HbA) [44]. Wen и сътр. въвеждатдве отделни точкови мутации 58T и 69A/70A като маркери за проследяване в HbS чрез CRISPR. В резултат на тези генетични отличителни белези, резултатът от генното редактиране наβ-глобиновия ген е лесно идентифициран по време на секвенирането. Важното е, че наличието на две отличителни белези на последователността в HBB изключва възможността за експериментално замърсяване, неочаквана вариация на генома или изкуствени мутации на последователността. Анализът на секвенирането показа, че тези генетични отличителни белези (58T и 70A) винаги са присъствали едновременно и са били открити във всички редактирани от генома клонинги; въпреки че двете места на мутация са на повече от 10 нуклеотида. Тези открития показват, че е възможно едновременно да се редактират две отделни целеви места в един и същ ген чрез подхода CRISPR/Cas9, като се използва една двойка sgRNA и HDR шаблон. Едновременното редактиране на геном на две целеви места може да бъде полезно за лечение на заболявания, носещи две или повече места на точкови мутации, които са близо едно до друго [45].
Използвайки индуцирани човешки плурипотентни стволови клетки (iPSC) от двама пациенти с β-таласемия с различни мутации на HBB гени, Cai и сътр. 2018 г. разработват и тестват универсална стратегия за постигане на целенасочено вмъкване на HBD cDNA в екзон 1 на гена HBB, използвайки Cas9 и две валидирани водещи РНКи. Те наблюдават, че производството на HBB протеин е възстановено в еритроцитите, получени от iPSC на двамата пациенти. Тази стратегия за възстановяване на функционална HBB генна експресия ще бъде в състояние да коригира повечето видове HBB генни мутации при β-таласемия и SCA [46].
Мутацията на CRYGC ген е автозомно доминираща мутация, която причинява пулверулентна катаракта. След коинжектиране в миши зиготи на Cas9 иРНК и единична направляваща РНК (sgRNA), насочена към мутантния алел, получените мишки са били плодовити и са били в състояние да предадат коригирания алел на своето потомство. По този начин изследването на Wu и сътр. предоставя принципно доказателство за използването на системата CRISPR-Cas9 за коригиране на генетично заболяване [47].
MYBPC3 участва в хипертрофичната кардиомиопатия – заболяване, което прави сърдечния мускул по-дебел. Това може да доведе до внезапна сърдечна недостатъчност и смърт при млади, иначе здрави спортисти, когато претоварват сърцата си твърде много, докато тренират. Мутацията е доминираща, което означава, че детето трябва да наследи само едно копие на мутиралия ген, за да изпита ефектите му. Болестта може да бъде овладяна с различни лечения, но реално лечение няма. Наскоро репродуктивният биолог Шухрат Миталипов и неговият екип използваха редактиране на генома, за да коригират ген, който причинява потенциално фатално сърдечно състояние при хората. Международен екип от изследователи използва CRISPR-Cas9 генна редакция, за да коригира болестотворна мутация в десетки жизнеспособни човешки ембриони. Ако оплодят ооцит със сперматозоиди, носещи мутант MYBPC3 заедно с Cas9 протеин, sgRNA и ДНК шаблон, оплодените яйца започват да произвеждат ембриони с два здрави гена MYBPC3 в 42 от 58 опити (над 70% от случаите), сравняващи контролния експеримент без CRISPR резултатът е около 50/50 [48].
Мускулната дистрофия на Дюшен (DMD) е тежко мускулно-дегенеративно заболяване, причинено от мутация в гена на дистрофин. Генетичната корекция на индуцирани от пациента плурипотентни стволови клетки (iPSCs) чрез TALEN или CRISPR-Cas9 обещава за DMD генна терапия; трябва обаче да се определи безопасността на такова лечение с нуклеаза. За възстановяване на дистрофиновия протеин Le и сътр. пробвали три метода за корекция (прескачане на екзон, изместване на рамката на четене и промяна на ДНК последователности) в получени от DMD iPSCs. Kоригираните iPSCs успешно се диференцирали в скелетни мускулни клетки и синтезирали дистрофинов протеин с нормална структура и функция [49].
Мускулните стволови клетки (MuSCs) притежават голям терапевтичен потенциал за мускулни генетични нарушения, като мускулна дистрофия на Дюшен (DMD). Zhu, et al. използват фибрин-гел културална система за селективно отглеждане на MuSCs от сурови скелетни мускулни клетки на mdx мишки (миши модел на DMD), в която след редактиране на генома чрез CRISP/Cas9 коригират мутацията на дистрофин в култивирани MuSCs и след трансплантацията им на mdx мишки възстановияват експресията на дистрофин в скелетните мускули на мишките [50]. Тези резултати осигуряват важна рамка за разработване на iPSC-базирана генна терапия за генетични заболявания, използващи програмируеми нуклеази. Техните проучвания установяват надеждна и осъществима платформа за генна корекция в MuSCs чрез редактиране на генома, като по този начин значително подобряват терапиите на базата на тъканни стволови клетки за DMD и други мускулни разстройства.
Изолираните човешки острови на панкреаса са рядък и ценен материал за изследване на диабета. Наличието им обаче е ограничено и е невъзможно да се получат от пациенти със специфични генотипове. Човешките плурипотентни стволови клетки осигуряват алтернатива. Индуцирани плурипотентни стволови клетки могат да бъдат генерирани от соматични клетки на всеки индивид и диференцирани в панкреасни клетки. Понастоящем този подход е ограничен от незрялостта на островоподобните клетки, получени от стволови клетки. Този подход обаче вече може да се използва за моделиране на дефекти в развитието и възможностите за изучаване на секрецията на инсулин непрекъснато се подобряват. В допълнение, редактирането на генома с помощта на технологията CRISPR/Cas9 предоставя мощни възможности за изследване на въздействието на специфични генотипове. Същата технология може да се използва и за регулиране на транскрипцията, за да се подобри функционалното съзряване на островчета, получени от стволови клетки. Днес тези подходи и методи стават достъпни за утрешно изследване на диабета. Използвайки CRISPR Gimenez и сътр. постигат активиране на човешки инсулинов ген във фибробласти, изолирани от пациенти с диабет тип 1 [51]. Същата година е публикуван първият доклад, демонстриращ подобрен диабет тип 1 при мишки чрез моделиране на PTPN22 (R620W) и полезността на CRISPR-Cas9 за директни генетични промени в NOD (незатлъстели диабетни) мишки [52]. Използването на CRISPR/Cas9 в плъхове LEW.1WR1 с T1D диабет тип 1 намалява появата на индуциран от вируса на Kilham диабет, което подкрепя използването на стратегии за ограничаване или предотвратяване на развитието на диабет тип 1 [53]. Ratiu и сътр. установили, че възстановяването на нормалната функция на гена чрез CRISPR/Cas9, индуциран от активирането на цитидин дезаминаза, инхибира развитието на диабет тип 1 в NOD мишки. Индуцираният от активирането ензим цитидин деаминаза предизвиква разкъсвания на ДНК в целия геном, които, ако не бъдат възстановени чрез RAD51-медиирана хомоложна рекомбинация, водят до смърт на В лимфоцити. Лечението с RAD51 инхибитор 4,4′-диизотиоцианатостилбен-2, 2′-дисулфонова киселина също силно инхибира развитието на диабет тип 1 при NOD мишки. Подходите за генетично манипулиране с малки молекули, активиращи CD73 + B лимфоцитите, които упражняват регулаторна активност, потискайки диабетогенните Т-клетъчни отговори чрез CRISPR/Cas9-медииран подход за генетична модификация идентифицира оста AID/RAD51 като цел за потенциално клинично ефективен фармакологичен подход, който може да блокира развитието на диабет тип 1 [54].
Чрез CRISPR/Cas9 технологията бяха инактивирани протеинови тирозин фосфатази PTPN6 и PTPN1 в човешки лангерхансови острови и островчета от NOD мишки. Авторите идентифицират PTPN6 като отрицателен регулатор на TNF-α-индуцирана смърт на β-клетки чрез JNK-зависимо разграждане на BCL-2 протеин. За разлика от това PTPN1 действа като положителен регулатор на IFN-y-индуцирана STAT1-зависима генна експресия, която засилва автоимунното разрушаване на β-клетките. Важно е, че инактивирането на PTPN1 предпазва β-клетките от медиирана от цитокини клетъчна смърт [55].
Чрез CRISPR/Cas9 медииран нокаут на ZnT8 Merriman et al. демонстрират, че ZnT8 е автоантиген на клетъчната повърхност, повишавайки възможността за пряко участие в медиирана от антитела β-клетъчна дисфункция и цитотоксичност [56]. Чрез технологията CRISPR-Cas9 са изследвани функциите на GPRC5B рецептора в β-клетките [57].
Технологията CRISPR/Cas9 стана привлекателна за лечение на ХИВ [58].
Гликопротеинът HIV-1 Env е локализиран в ендоплазмения ретикулум (ER), който е необходим за попадане и репликация на вируса. Чрез CRISPR/Cas9 беше нокаутиран TSPO гена в 293T клетки и беше установено, че TSPO може по подобен начин да инхибира Env експресията в тези клетки [59].
Хора, хомозиготни за гена C-C хемокинов рецептор тип 5 с 32-bp делеции (CCR5Δ32), са резистентни към HIV-1 инфекция. Ye и сътр. генерират плурипотентни стволови клетки (iPSCs), хомозиготни за естествено срещащата се CCR5Δ32 мутация чрез геномно редактиране на iPSCs от див тип, използвайки комбинация от транскрипционни активатор-подобни ефекторни нуклеази (TALENs) или РНК-ръководени клъстерирани редовно взаимосвързани къси палиндромни повторения (CRISPR) – Cas9 заедно с технологията piggyBac. Тези модифицирани iPSCs в моноцити/макрофаги демонстрира устойчивост на HIV-1. Авторите предполагат, че тази стратегия може да осигури подход към функционално излекуване от HIV-1 инфекция [60].
CCR5 служи като съществен ко-рецептор за навлизане на вируса на човешка имунна недостатъчност тип 1 (HIV-1), а индивидите с вариант CCR5 (Δ32) изглеждат здрави, което прави CCR5 привлекателна цел за контрол на HIV-1 инфекцията. CCR5 ко-рецепторът за навлизане на HIV-1, е основна цел за лекарствена и генетична намеса срещу HIV-1. Wang и сътр. инхибират CCR5 чрез CRISPR/Cas9. Те конструират лентивирусни вектори, експресиращи Cas9 и CCR5 sgRNAs. В резултат CCR5 генно-разрушените клетки са не само устойчиви на R5-тропния HIV-1, но също така имат селективно предимство пред CCR5 генно-нарушените клетки по време на R5-тропната HIV-1 инфекция. Заглушаването или нарушаването на CCR5 чрез Cas9 и CCR5-специфични sgRNAs може да бъде жизнеспособна алтернативна стратегия за инженерна резистентност срещу HIV-1 [61,62]. Li и сътр. конструират химерни Ad5F35 аденовируси, носещи компоненти CRISPR/Cas9, ефективно трансдуцирани първични CD4 (+) Т-лимфоцити с нарушена експресия на CCR5. Трансдуцираните първични CD4 (+) Т-клетки са устойчиви на HIV-1 [63].
Трансплантацията на хематопоетични стволови клетки (HSC) с естествена CCR5 мутация носи загуба на откриваем HIV-1 при пациента. Възстановяването на нормалнаа функция на гена CCR5 в HSCs е идеална терапия за лечение на HIV-1. Xu и сътр. създават система за редактиране на ген с CRISPR/Cas9 в човешки CD34 + HSPC и постигат ефективна репарация на CCR5, която придава резистентност към HIV-1 in vivo. Тази стратегия предлага терапия чрез трансплантация на CCSC5, редактиран от CCR5, за лечение на ХИВ в клиниката [64].
CXCR4 е също ко-рецептор за инфекция с вирус на човешка имунна недостатъчност тип 1 (HIV-1) и се счита за важна терапевтична цел за СПИН. CXCR4 медиира вирусното навлизане в човешки CD4 (+) клетки чрез свързване с обвиващ протеин gp120. Разрушаването на човешкият ген CXCR4 чрез CRISPR/Cas9-медиирано редактиране на генома води до HIV-1 резистентност на човешки първични CD4 (+) Т клетки. Прецизното и ефективно редактиране на генома на CXCR4 ще осигури и нова стратегия за терапевтично приложение срещу HIV-1 инфекция [65]. Напоследък е разработен малък Staphylococcus aureus Cas9 (SaCas9) като инструмент за редактиране на генома. Той предоставя обещаваща стратегия за HIV-1 генна терапия, ако се използва за насочване към CXCR4. Wang и сътр. демонстрират, че трансдукцията на лентивирус, експресиращ SaCas9 и избрани еднонасочени РНК на CXCR4 в човешки CD4 + Т клетъчни линии ефективно индуцира редактирането на гена CXCR4 и нарушава експресията на CXCR4, правейки тези клетъчни линии устойчиви на X4-тропична HIV-1 инфекция. Редактираните с CXCR4 първични CD4 + Т клетки се разпространяват нормално и са устойчиви на HIV-1 инфекция [66].
Нарушаването или на CCR5 или на CXCR4 дава резистентност към HIV-1 инфекция. Въпреки това спешната необходимост от премахване на двата ко-рецептора за двойна защита остава. Yu и сътр. Успешно възстановяват гените CCR5 и CXCR4 в човешки CD4 + клетъчни линии и първични CD4 + Т клетки едновременно, използвайки CRISPR Cas9. Резултатите демонстрират безопасността и ефикасността на CRISPR/Cas9 при мултиплексна генна модификация на периферно циркулиращи CD4 + Т клетки, което може да насърчи функционално излекуване за HIV-1 инфекция [67]. Едновременното редактиране на геном на CXCR4 и CCR5 от CRISPR-Cas9 може потенциално да осигури ефективна и безопасна стратегия за функционално излекуване на HIV-1 инфекция [68].
Редактирането на гени с помощта на CRISPR/Cas9 може да осигури нов терапевтичен път за елиминиране на HIV-1 ДНК от CD4 + Т-клетки и потенциално да служи като нова и ефективна платформа за лечение на СПИН [69].
CRISPR-Csy4 ендорибонуклеазата също е обещаващ инструмент, който може да бъде адаптиран допълнително за насочване към ХИВ-1 [70].
Нова каталитично-дефицитна Cas9-синергична медиаторна активация (dCas9-SAM) може да послужи като нов терапевтичен инструмент за обръщане на латентността на HIV за трайно елиминиране на латентни резервоари на HIV-1 [71].
Генспецифичната транскрипционна активация може да бъде постигната с помощта на РНК-ръководена система CRISPR-Cas9, включваща единични РНК (sgRNAs) с нуклеазно-дефицитен Cas9 мутант (dCas9), слети с VP64 трансактивационния домейн (dCas9-VP64). Тази система е проектирана да насочва към 23 места в дългия терминален повторен промотор на HIV-1 и идентифицира „гореща точка“ за активиране в последователността на вирусния енхансер на генната експресия [72]. Също така системата dCas9-SunTag-VP64 може ефективно и конкретно да активира латентна транскрипция на HIV-1, което предполага, че тази стратегия може да предложи нов подход към латентността срещу HIV-1 [73].
Пълното унищожаване на HIV-1 инфекцията е възпрепятствано от съществуването на клетки, които съдържат хромозомно интегриран, но транскрипционно неактивен провирус. Тези клетки могат да съществуват с години, без да произвеждат вирусно потомство, което ги прави рефрактерни към имунното наблюдение и антиретровирусната терапия, осигурявайки постоянен резервоар за стохастично реактивиране и повторно намножаване на HIV-1. Поради това са необходими стратегии за прочистване на този скрит резервоар за ликвидиране на инфекцията. Системите CRISPR са потенциално ефективни инструменти за индуциране на латентна експресия на HIV-1 и в комбинация с антиретровирусна терапия могат да доведат до подобрени терапии за HIV-1 инфекция [74].
Използвайки HIV-1 инфекцията като модел, Liao и сътр. демонстрират, че системата CRISPR/Cas9 нарушава латентно интегрирания вирусен геном и осигурява дългосрочна адаптивна защита срещу нова вирусна инфекция, експресия и репликация в човешки клетки. Тези резултати разкриват потенциала на системата CRISPR/Cas9 като нова терапевтична стратегия срещу вирусни инфекции [75].
Мутираният от CRISPR/Cas9 целеви сайт във втория екзон, наречен T10, води до значително намалена експресия на гена на HIV-1 и производство на вируси в латентно инфектирани Jurkat клетки. Това разкрива високоефективен целеви сайт Cas9 във втория екзон на Rev, който представлява обещаваща цел, която следва да бъде проучена допълнително в CRISPR/Cas9-базирана стратегия за лечение [76].
Камински и др. демонстрират, че функционалното активиране на CRISPR/Cas9 от Tat по време на вирусна инфекция изрязва определения сегмент на интегрираната вирусна ДНК и следователно потиска вирусната експресия [77].
Стратегията за редактиране на ген CRISPR/Cas9 е забележителна при заразени човешки клетъчни линии. Камински и др. инжектират в опашната вена кратка версия на Cas9 ендонуклеазата saCas9 заедно с мултиплекс от направляващи РНК (gRNAs) за насочване на HIV-1 ДНК последователностите в 5′-LTR и Gag гена за отстраняване на критично важни сегменти в трансгенни мишки и плъхове, обхващащи генома на HIV-1. Тези резултати за първи път демонстрират in vivo ликвидирането на ДНК на HIV-1 чрез CRISPR/Cas9 [78]. In vivo изрязването на HIV-1 провирусна ДНК чрез sgRNAs/saCas9 в твърди тъкани/органи при мишки може да бъде постигната чрез доставка на AAV, е значителна стъпка към клинични изпитвания при хора [79].
Астроцитите, най-разпространените глиални клетки в мозъка на бозайниците, изпълняват ключови функции и участват в няколко невродегенеративни заболявания. Вирусът на човешката имунна недостатъчност (ХИВ) може да инфектира астроцитите, допринасяйки за тежестта на ХИВ и неврологичните дисфункции при заразените индивиди. Huang и Nair създават нов, прост и бърз скрининг метод за идентифициране на кандидати за gRNA за насочване на ХИВ провирус в астроцитите [80]. Съобщава се за нов адено-свързан вирус-базиран вектор (AAV9P1) със синтетичен повърхностен пептид за трансдукция на астроцити като инструмент за доставяне на ХИВ-инхибиторни гени в астроцитите. Kunze и сътр. генерират AAV9P1 вектори, съдържащи гени за HIV-1 провирусно редактиране от CRISPR/Cas9. Латентно заразените с HIV-1 астроцити, трансдуцирани с тези вектори, показват значително намалено реактивиране на провирусите в сравнение с нетрансдуцирани култури. AAV9P1 е обещаващ инструмент за доставка на гени до астроцитите и може да улесни инактивирането/унищожаването на персистиращи HIV-1 провируси в резервоарите за астроцити [81].
Към днешна дата анти-HIV-1 gRNAs са проектирани да насочват към определена последователност, но те рядко отчитат генетичните вариации в генома на HIV-1 в рамките и между пациентите, което ще бъде от решаващо значение за терапевтичното приложение на тази технология. Dampier и сътр. създават основни изчислителни инструменти за анализ на получените от пациента HIV-1 последователности, за да се получи информация за дизайна на gRNA [82].
Индуцируемият тип I интерферон (IFN-I) човешки рестрикционен фактор TRIM5α инхибира инфекцията на човешки клетки от специфични нечовешки ретровируси, като N-MLV и EIAV, но като цяло не е насочен към HIV-1. Въпреки това, въвеждането на две аминокиселинни замествания, R332G и R355G, в човешкия TRIM5α (huTRIM5α) домейн, отговорен за разпознаването на ретровирусни капсиди, води до ефективно ограничаване на HIV-1 при стабилна свръхекспресия. Чрез CRISPR-Cas9 беше успешно мутиран TRIM5 до неговата потенциално HIV-1-рестриктивна версия чрез хомоложно насочена реконструкция (HDR) в клетки HEK293T. Редактирането на гена TRIM5 идентифицира ново предизвикателство, за да се използва този подход за осигуряване на защита от ХИВ-1 [83].
Експериментално изчерпване на USP18 от CRISPR-Cas9 води до значително ограничаване на репликацията на HIV-1 в индуциран модел на макрофаги, произведен от плурипотентни стволови клетки (iPSC) [84].
Потискането на ХИВ-1 от CRISPR/Cas9 има предимства и недостатъци. Ранните експерименти с RNAi демонстрират дълбоко инхибиране на вируса, но също така показват, че е възможно вирусно бягство. Има наблюдения, които илюстрират противоположни резултати от ефекта на CRISPR/Cas9 при инактивиране на HIV-1, което потенциално ограничава използването на CRISPR/Cas9 при терапия с HIV-1 [85-88]. ХИВ вирусът може да произведе щамове, устойчиви на CRISPR/Cas9 [89].
Съществуват потенциални трудности, на които трябва да се обърне внимание, когато се обмисля лечение срещу HIV-1 само със системата CRISPR/Cas9. HIV-1 може да избяга от единична антивирусна gRNA чрез мутация на прицелната последователност. Комбинациите от две антивирусни gRNAs забавят вирусното бягство [90,91].
Но понякога трябва да се внимава много и с комбинираните подходи [92].
След няколко десетилетия терапията с CRISPR може да излекува ХИВ и ретровируси, вируси, които се крият в човешката ДНК, могат да бъдат унищожени [93-100] и би могла да служи успешно за лечение на рак [101-105].
Програмираният с РНК Cas9 може да предложи значителен потенциал за редактиране на генома в клетки от трите царства на живота за биотехнологични, биомедицински и генно-терапевтични цели. CRISPR/Cas9 може да помогне за разбирането на функциите на гените и да разкрие нови пътища, проектиране на модели на болести, скрининг за нови цели за терапевтични средства, генетично предразположение към заболявания, генна терапия. Необходимо е внимание за разкриване на някои рискове от CRISPR/Cas9 индуцирани инсерционни или делеционни мутации [106,107].
Ding, et al. съобщават, че поправката на разцепването на и извън целта е довело до голямо разнообразие от инсерции, делеции и точкови мутации. Следователно системите CRISPR/Cas9 трябва да бъдат внимателно проектирани, за да се избегнат неочаквани места за разцепване.
Редактирането на генома със системата CRISPR/Cas9 разрушава гена Pcsk9 in vivo с висока ефективност и намалява нивата на холестерола в кръвта при мишки. Този подход може да има терапевтичен потенциал за профилактика на сърдечно-съдови заболявания при хората [108].
РНК-насоченото разрушаване на гените чрез CRISPR/Cas на целевата ДНК е мощен подход за целенасочено генно разрушаване при различни животински модели [109].
Въпреки това има малко данни за ефективността на методите за микроинжектиране и за генериране на нокаутирани мишки чрез този подход. Horii и сътр. сравняват три метода за инжектиране: (1) инжектиране на ДНК в пронуклеуса, (2) инжектиране на РНК в пронуклеуса и (3) инжектиране на РНК в цитоплазмата. Те откриват, че инжектирането на РНК в цитоплазмата е най-ефективният метод от гледна точка на броя на жизнеспособните ембриони от стадия на бластоциста и генерираните доносени малки. Този метод също показа най-добрата цялостна ефективност при индуцирането на нокаут мутации[110].
Етични въпроси
Тази технология е изключително добро средство при лечението на генетични заболявания и вируси в човешкия геном. За да останат тези промени трайни и да се предадат на следващото поколение, е необходимо да се модифицират гени или ембриони. Но възниква случаят: ако е възможно да се промени човешкият геном за лечение на заболявания, защо да не е възможно да се променят характеристиките на плода по желание на родителите. Ако това е позволено, възможно е разнообразието от гени в геномния пул да намалее и разнообразието на човешкия вид да изчезне. Друг вариант е да се обърне процесът на стареене и да се премахнат старите заболявания.
Свят без болести? Потенциално мощно приложение за разработването на устойчиви на болести комари, напр. малария и зика.
Редактирането на гени вече може да промени цял вид завинаги. CRISPR позволява на учените да променят последователностите на ДНК и гарантира, че получената редактирана генетична характеристика се наследява от бъдещите поколения, отваряйки възможността за промяна на цели видове завинаги. Повече от всичко тази технология води до въпроси: Как тази нова сила ще повлияе на човечеството? Какво ще използваме, за да го променим? Сега богове ли сме? Бъдещето на CRISPR ще бъде новата ера за човечеството. Генното инженерство ще промени всичко завинаги, тъй като тази техника може да направи много неща за генното инженерство и е приемлива за много хора. И най-вече това е наистина наистина вълнуващо.
CRISPR е много мощен инструмент, който се нуждае от много съзерцание относно неговите последици. Една малка грешка може да доведе до катастрофа.
С изключение на лечението на заболявания, CRISPR може и вероятно ще се използва за много повече: създаването на модифицирани хора – дизайнерски бебета – и ще означава постепенни, но необратими промени в човешкия генофонд. Първите проектирани бебета ще бъдат създадени за премахване на смъртоносни генетични заболявания, предаващи се в семейството. С напредването на технологията и усъвършенстването, все повече хора ще я използват. Веднага щом се роди първото конструирано дете, врата се отваря и не може да бъде затворена повече. От природата знаем, че има животни, имунизирани срещу стареене. Може би дори бихме могли да заемем няколко гена от тях. Предизвикателствата са огромни. Дизайнерски бебета, краят на болестите, генетично модифицирани хора, които никога не остаряват. Скандални неща, които преди бяха научна фантастика, изведнъж се превръщат в реалност. Единственото, което знаем със сигурност е, че нещата ще се променят необратимо. Но въпреки революцията CRISPR/Cas9 сега е за наука, все още е само инструмент от първо поколение.
Заключения
CRISPR променя цялото поле на биологията. Използвайки тази техника, учените могат да редактират гени с точност и скорост, каквито никога преди не са имали. Възможно е да промените броя на някои специфични гени в клетката или да го изтриете напълно. Възможно е също да се направи мутация в ген чрез промяна, добавяне или изваждане на парчета ДНК или единични нуклеотиди. Или можете да въведете ген от съвсем различен организъм. Подобно на това как правим бактерии, които синтезират инсулин и използваме гена за GFP – светещия зелен протеин от медузи като биомаркер в много експерименти. Има няколко техники, но нито една от тях не е толкова удобна. Например чрез трансфекция клетките ще експресират гена за няколко дни, но той не е част от хромозома, така че не можете да сте сигурни, че функцианира нормално. Можете също така да използвате модифициран вирус, за да доставите ген, тъй като те обикновено интегрират своя генетичен материал в ДНК на гостоприемника. Този метод обаче има проблеми: вирусът не се интересува къде интегрира новия ген, така че може да се удари в средата на друг ген и да причини куп проблеми. Промяната на цял организъм, като изтриване на ген при мишки, може да отнеме години, хиляди долари, поколения от разплод и късмет. CRISPR/Cas9 е система, при която можете да изпратите един протеин за точно прерязване навсякъде в генома, само като му дадете парче РНК. Клетката използва шаблон за възстановяване на ДНК. Възможно е да изпратите шаблон заедно с РНК и Cas9, така че той добавя каквото искате, като изцяло нов ген например. Тъй като шаблоните са насочени към определена част от генома, ще имате точното количество от вашия ген, интегрирано в хромозома за разлика от по-старите техники, при които получавате твърде много копия или дори твърде малко. Така че CRISPR/Cas9 прави редактирането на гени по-бързо, по-евтино и по-точно отколкото преди.
Но както всяка техника, системата CRISPR/Cas9 не е перфектна. Понякога се реже на грешното място. Може да се придържа към последователност, която почти съвпада с направляващата РНК. В отгледаните в лаборатории клетки това не е огромен проблем. Възможно е да използвате техниката няколко пъти и да проверите за клетка, в която е направено правилно, и все пак е много по-точен от други методи. Но лекарите също започват да разработват CRISPR/Cas9 като генна терапия за пациенти. Погрешното езменение на генома на вече болен човек може да бъде катастрофално. Ако имат рак, например, допълнително повреден ген във вече мутиралите клетки може да влоши болестта. Ето защо учените внимателно сатрябва да проектират водещата РНК и аминокиселинната последователност на Cas9, за да се опитат да направят техниката по-точна и да изрязват правилната последователност всеки път. Клиничните изпитвания върху хора, включващи CRISPR/Cas9, си проправят път през процеса на одобрение: един в университета в Пенсилвания в САЩ и един в университета в Съчуан в Китай. И двете комбинират CRISPR Cas9 с друго лечение на рак – имунотерапия. И двете проучвания ще вземат някои от имунните клетки на пациента и ще използват CRISPR/Cas9, за да им дадат генетичен тласък за разпознаване на ракови клетки. След това имунните клетки ще се върнат в пациента, за да могат да започнат работа. Изследователите очакват методът CRISPR/Cas9 да работи още по-добре. Освен редактирането на гени в клетките на възрастен индивид, CRISPR/Cas9 дава на учените силата да редактират човешки ембриони.
Правени са също така са опити, използващи CRISPR/Cas9, за да убият или да променят генома на комари, предаващи малария, за да не могат да разпространяват маларийния плазмодий.
Но ако хората вече могат да манипулират генома на който и да е организъм, има етични въпроси, които трябва да разгледаме. Очаква се бързият напредък в технологията CRISPR/Cas9 да намали и в крайна сметка да елиминира риска от нецелеви генни ефекти, а CRISPR/Cas9 ще се превърне в стандартния метод за лечение на генетични нарушения в рутинната клинична практика.
Засега CRISPR/Cas9 се използва най-вече за редактиране на геноми в клетки в клетъчни култури, за да се изследва как функционират без ген или с нов ген.
Литература
- Ishino Y, Shinagawa H, Makino K, Amemura M, Nakata A (1987) „Nucleotide sequence of the iap gene, responsible for alkaline phosphatase isozyme conversion in Escherichia coli, and identification of the gene product“. J Bacteriol 169: 5429-5433.
- Mojica FJ, Juez G, Rodriguez-Valera F (1993) Transcription at different salinities of Haloferax mediterranei sequences adjacent to partially modified PstI sites. Mol Microbiol 9: 613-621.
- Jansen R, Embden JD, Gaastra W, Schouls LM (2002) Identification of genes that are associated with DNA repeats in prokaryotes. Mol Microbiol 43: 1565-1575. [Crossref]
- Bolotin A, Quinquis B, Sorokin A, Ehrlich SD (2005) Clustered regularly interspaced short palindrome repeats (CRISPRs) have spacers of extrachromosomal origin. Microbiology 151: 2551-2561.
- Barrangou R, Fremaux C, Deveau H, Richards M, Boyaval P, et al. (2007) CRISPR provides acquired resistance against viruses in prokaryotes. Science 315: 1709-1712.
- Marraffini LA, Sontheimer EJ (2009) Invasive DNA, chopped and in the CRISPR. Structure 17: 786-788. [Crossref]
- van der Oost J, Jore MM, Westra ER, Lundgren M, Brouns SJ (2009) CRISPR-based adaptive and heritable immunity in prokaryotes. Trends Biochem Sci 34: 401-407. [Crossref]
- Horvath P, Barrangou R (2010) CRISPR/Cas, the immune system of bacteria and archaea. Science 327: 167-170. [Crossref]
- Hale CR, Zhao P, Olson S, Duff MO, Graveley BR, et al. (2009) RNA-guided RNA cleavage by a CRISPR RNA-Cas protein complex. Cell 139: 945-956. [Crossref]
- Marraffini LA, Sontheimer EJ (2010) Self versus non-self discrimination during CRISPR RNA-directed immunity. Nature 463: 568-571. [Crossref]
- Marraffini LA, Sontheimer EJ (2010) CRISPR interference: RNA-directed adaptive immunity in bacteria and archaea. Nat Rev Genet 11: 181-190. [Crossref]
- Karginov FV, Hannon GJ (2010) The CRISPR system: small RNA-guided defense in bacteria and archaea. Mol Cell 37: 7-19. [Crossref]
- Garneau JE, Dupuis MÈ, Villion M, Romero DA, Barrangou R, et al. (2010) The CRISPR/Cas bacterial immune system cleaves bacteriophage and plasmid DNA. Nature 468: 67-71. [Crossref]
- Babu M, Beloglazova N, Flick R, Graham C, Skarina T, et al. (2011) A dual function of the CRISPR-Cas system in bacterial antivirus immunity and DNA repair. Mol Microbiol 79: 484-502. [Crossref]
- Sapranauskas R, Gasiunas G, Fremaux C, Barrangou R, Horvath P, et al. (2011) The Streptococcus thermophilus CRISPR/Cas system provides immunity in Escherichia coli. Nucleic Acids Res 39: 9275-9282.
- Gasiunas G, Barrangou R, Horvath P, Siksnys V (2012) Cas9-crRNA ribonucleoprotein complex mediates specific DNA cleavage for adaptive immunity in bacteria. Proc Natl Acad Sci USA 109: E2579-E2586.
- Jinek M, Chylinski K, Fonfara I, Hauer M, Doudna JA, et al. (2012) A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity. Science 337: 816-821. [Crossref]
- Pollack, Andrew (2015) Jennifer Doudna, a Pioneer Who Helped Simplify Genome Editing“. New York Times.
- Barrangou R, Doudna JA (2016) Applications of CRISPR technologies in research and beyond. Nat Biotechnol 34: 933-941. [Crossref]
- Hwang WY, Fu Y, Reyon D, Maeder ML, Tsai SQ, et al. (2013) Efficient genome editing in zebrafish using a CRISPR-Cas system. Nat Biotechnol 31: 227-229. [Crossref]
- Hwang WY, Fu Y, Reyon D, Maeder ML, Kaini P, et al. (2013) Heritable and precise zebrafish genome editing using a CRISPR-Cas system. PLoS One 8: e68708. [Crossref]
- Ota S, Hisano Y, Ikawa Y, Kawahara A (2014) Multiple genome modifications by the CRISPR/Cas9 system in zebrafish. Genes Cells 19: 555-564. [Crossref]
- Kimura Y, Hisano Y, Kawahara A, Higashijima S (2014) Efficient generation of knock-in transgenic zebrafish carrying reporter/driver genes by CRISPR/Cas9-mediated genome engineering. Sci Rep 4: 6545.
- Cho SW, Kim S, Kim JM, Kim JS (2013) Targeted genome engineering in human cells with the Cas9 RNA-guided endonuclease. Nat Biotechnol 31: 230-232. [Crossref]
- Jinek M, East A, Cheng A, Lin S, Ma E, et al. (2013) RNA-programmed genome editing in human cells. Elife 2: e00471. [Crossref]
- Fu Y, Foden JA, Khayter C, Maeder ML, Reyon D, et al. (2013) High-frequency off-target mutagenesis induced by CRISPR-Cas nucleases in human cells. Nat Biotechnol 31: 822-826. [Crossref]
- Maeder ML, Linder SJ, Cascio VM, Fu Y, Ho QH, et al. (2013) CRISPR RNA-guided activation of endogenous human genes. Nat Methods 10: 977-979. [Crossref]
- Bassett AR, Tibbit C, Ponting CP, Liu JL (2013) Highly efficient targeted mutagenesis of Drosophila with the CRISPR/Cas9 system. Cell Rep 4: 220-228.
- Yu Z, Ren M, Wang Z, Zhang B, Rong YS, et al. (2013) Highly efficient genome modifications mediated by CRISPR/Cas9 in Drosophila. Genetics 195: 289-291.
- Xie K, Yang Y (2013) RNA-guided genome editing in plants using a CRISPR-Cas system. Mol Plant 6: 1975-1983. [Crossref]
- Feng Z, Zhang B, Ding W, Liu X, Yang DL, et al. (2013) Efficient genome editing in plants using a CRISPR/Cas system. Cell Res 23: 1229-1232. [Crossref]
- Gilbert LA, Larson MH, Morsut L, Liu Z, Brar GA, et al. (2013) CRISPR-mediated modular RNA-guided regulation of transcription in eukaryotes. Cell 154: 442-451. [Crossref]
- Mao Y, Zhang H, Xu N, Zhang B, Gou F, et al. (2013) Application of the CRISPR-Cas system for efficient genome engineering in plants. Mol Plant 6: 2008-2011. [Crossref]
- Walsh RM, Hochedlinger K (2013) A variant CRISPR-Cas9 system adds versatility to genome engineering. Proc Natl Acad Sci USA 110: 15514-15515. [Crossref]
- Zhonggang Hou, Yan Zhang, Nicholas EP, Sara EH, Li-Fang Chu, et al. (2013) Efficient genome engineering in human pluripotent stem cells using Cas9 from Neisseria meningitides. Proc Natl Acad Sci USA 110: 15644-15649.
- Wu X, Scott DA, Kriz AJ, Chiu AC, Hsu PD, et al. (2014) Genome-wide binding of the CRISPR endonuclease Cas9 in mammalian cells. Nat Biotechnol 32: 670-676. [Crossref]
- Schmid B, Haass C (2013) Genomic editing opens new avenues for zebrafish as a model for neurodegeneration. J Neurochem 127: 461-470. [Crossref]
- Wilkinson RN, Jopling C, van Eeden FJ (2014) Zebrafish as a model of cardiac disease. Prog Mol Biol Transl Sci 124: 65-91. [Crossref]
- Choi PS, Meyerson M (2014) Targeted genomic rearrangements using CRISPR/Cas technology. Nat Commun 5: 3728. [Crossref]
- Horii T, Morita S, Kimura M, Kobayashi R, Tamura D, et al. (2013) Genome engineering of mammalian haploid embryonic stem cells using the Cas9/RNA system. PeerJ 1: e230.
- Hsu PD, Lander ES, Zhang F (2014) Development and applications of CRISPR-Cas9 for genome engineering. Cell 157: 1262-1278. [Crossref]
- Huang X, Wang Y, Yan W, Smith C, Ye Z, et al. (2015) Production of Gene-Corrected Adult Beta Globin Protein in Human Erythrocytes Differentiated from Patient iPSCs After Genome Editing of the Sickle Point Mutation. Stem Cells 33: 1470-1479.
- Hoban MD, Lumaquin D, Kuo CY, Romero Z, Long J, et al. (2016) CRISPR/Cas9-Mediated Correction of the Sickle Mutation in Human CD34+ cells. Mol Ther 24: 1561-1569. [Crossref]
- Dever DP, Bak RO, Reinisch A, Camarena J, Washington G, et al. (2016) CRISPR/Cas9 β-globin gene targeting in human haematopoietic stem cells. Nature 539: 384-389. [Crossref]
- Wen J, Tao W, Hao S, Zu Y (2017) Cellular function reinstitution of offspring red blood cells cloned from the sickle cell disease patient blood post CRISPR genome editing. J Hematol Oncol 10: 119.
- Cai L, Bai H (2018) A Universal Approach to Correct Various HBB Gene Mutations in Human Stem Cells for Gene Therapy of Beta-Thalassemia and Sickle Cell Disease. Stem Cells Transl Med 7: 87-97. [Crossref]
- Wu Y, Liang D, Wang Y, Bai M, Tang W, et al. (2013) Correction of a genetic disease in mouse via use of CRISPR-Cas9. Cell Stem Cell 13: 659-662. [Crossref]
- Ma H, Marti-Gutierrez N, Park SW, Wu J, Lee Y, et al. (2017) Correction of a pathogenic gene mutation in human embryos. Nature 548: 413-419. [Crossref]
- Li HL, Fujimoto N, Sasakawa N, Shirai S, Ohkame T, et al. (2015) Precise correction of the dystrophin gene in duchenne muscular dystrophy patient induced pluripotent stem cells by TALEN and CRISPR-Cas9. Stem Cell Reports 4: 143-154.
- Zhu P, Wu F, Mosenson J, Zhang H, He TC, et al. (2017) CRISPR/Cas9-Mediated Genome Editing Corrects Dystrophin Mutation in Skeletal Muscle Stem Cells in a Mouse Model of Muscle Dystrophy. Mol Ther Nucleic Acids 7: 31-41.
- Giménez CA, Ielpi M, Mutto A, Grosembacher L, Argibay P, et al. (2016) CRISPR-on system for the activation of the endogenous human INS gene. Gene Ther 23: 543-547. [Crossref]
- Lin X, Pelletier S, Gingras S, Rigaud S, Maine CJ, et al. (2016) CRISPR-Cas9-Mediated Modification of the NOD Mouse Genome With Ptpn22R619W Mutation Increases Autoimmune Diabetes. Diabetes 65: 2134-2138.
- Qaisar N, Lin S, Ryan G, Yang C, Oikemus SR, et al. (2017) A Critical Role for the Type I Interferon Receptor in Virus-Induced Autoimmune Diabetes in Rats. Diabetes 66: 145-157. [Crossref]
- Ratiu JJ, Racine JJ, Hasham MG, Wang Q, Branca JA, et al. (2017) Genetic and Small Molecule Disruption of the AID/RAD51 Axis Similarly Protects Nonobese Diabetic Mice from Type 1 Diabetes through Expansion of Regulatory B Lymphocytes. J Immunol 198: 4255-4267.
- Stanley WJ, Trivedi PM, Sutherland AP, Thomas HE, Gurzov EN (2017) Differential regulation of pro-inflammatory cytokine signalling by protein tyrosine phosphatases in pancreatic ß-cells. J Mol Endocrinol 59: 325-337.
- Merriman C, Huang Q, Gu W, Yu L, Fu D (2018) A subclass of serum anti-ZnT8 antibodies directed to the surface of live pancreatic β-cells. J Biol Chem 293: 579-587. [Crossref]
- Atanes P, Ruz-Maldonado I, Hawkes R, Liu B, Persaud SJ, et al. (2018) Identifying Signalling Pathways Regulated by GPRC5B in ß-Cells by CRISPR-Cas9-Mediated Genome Editing. Cell Physiol Biochem 45: 656-666.
- Hu W, Kaminski R, Yang F, Zhang Y, Cosentino L, et al. (2014) RNA-directed gene editing specifically eradicates latent and prevents new HIV-1 infection. Proc Natl Acad Sci USA 111: 11461-11466.
- Zhou T, Dang Y, Zheng YH (2014) The mitochondrial translocator protein, TSPO, inhibits HIV-1 envelope glycoprotein biosynthesis via the endoplasmic reticulum-associated protein degradation pathway. J Virol 88: 3474-3484.
- Ye L, Wang J, Beyer AI, Teque F, Cradick TJ, et al. (2014) Seamless modification of wild-type induced pluripotent stem cells to the natural CCR5?32 mutation confers resistance to HIV infection. Proc Natl Acad Sci USA 111: 9591-9596.
- Wang W, Ye C, Liu J, Zhang D, Kimata JT, et al. (2014) CCR5 gene disruption via lentiviral vectors expressing Cas9 and single guided RNA renders cells resistant to HIV-1 infection. PLoS One 9: e115987.
- Kang H, Minder P, Park MA, Mesquitta WT, Torbett BE, et al. (2015) CCR5 Disruption in Induced Pluripotent Stem Cells Using CRISPR/Cas9 Provides Selective Resistance of Immune Cells to CCR5-tropic HIV-1 Virus. Mol Ther Nucleic Acids 4: e268.
- Li C, Guan X, Du T, Jin W, Wu B, et al. (2015) Inhibition of HIV-1 infection of primary CD4+ T-cells by gene editing of CCR5 using adenovirus-delivered CRISPR/Cas9. J Gen Virol 96: 2381-2393. [Crossref]
- Xu L, Yang H, Gao Y, Chen Z, Xie L, et al. (2017) CRISPR/Cas9-Mediated CCR5 Ablation in Human Hematopoietic Stem/Progenitor Cells Confers HIV-1 Resistance In Vivo. Mol Ther 25: 1782-1789. [Crossref]
- Hou P, Chen S, Wang S, Yu X, Chen Y, Jiang M, Zhuang K, Ho W, Hou W, Huang J, Guo D. (2015) Genome editing of CXCR4 by CRISPR/cas9 confers cells resistant to HIV-1 infection. Sci Rep 5: 15577.
- Wang Q, Chen S, Xiao Q, Liu Z, Liu S, et al. (2017) Genome modification of CXCR4 by Staphylococcus aureus Cas9 renders cells resistance to HIV-1 infection. Retrovirology 14: 51.
- Yu S, Yao Y, Xiao H, Li J, Liu Q, et al. (2018) Simultaneous Knockout of CXCR4 and CCR5 Genes in CD4+ T Cells via CRISPR/Cas9 Confers Resistance to Both X4- and R5-Tropic Human Immunodeficiency Virus Type 1 Infection. Hum Gene Ther 29: 51-67.
- Liu Z, Chen S, Jin X, Wang Q (2017) Genome editing of the HIV co-receptors CCR5 and CXCR4 by CRISPR-Cas9 protects CD4+ T cells from HIV-1 infection. Cell Biosci 7: 47. [Crossref]
- Kaminski R, Chen Y, Fischer T, Tedaldi E, Napoli A, et al. (2016) Elimination of HIV-1 Genomes from Human T-lymphoid Cells by CRISPR/Cas9 Gene Editing. Sci Rep 6: 22555.
- Guo R, Wang H, Cui J, Wang G, Li W, et al. (2015) Inhibition of HIV-1 Viral Infection by an Engineered CRISPR Csy4 RNA Endoribonuclease. PLoS One 10: e0141335. [Crossref]
- Zhang Y, Yin C, Zhang T, Li F, Yang W, et al. (2015) CRISPR/gRNA-directed synergistic activation mediator (SAM) induces specific, persistent and robust reactivation of the HIV-1 latent reservoirs. Sci Rep 5: 16277.
- Saayman SM, Lazar DC, Scott TA, Hart JR (2016) Potent and Targeted Activation of Latent HIV-1 Using the CRISPR/dCas9 Activator Complex. Mol Ther 24: 488-498. [Crossref]
- Ji H, Jiang Z, Lu P, Ma L, Li C (2016) Specific Reactivation of Latent HIV-1 by dCas9-SunTag-VP64-mediated Guide RNA Targeting the HIV-1 Promoter. Mol Ther 24: 508-521. [Crossref]
- Limsirichai P, Gaj T, Schaffer DV (2016) CRISPR-mediated Activation of Latent HIV-1 Expression. Mol Ther 24: 499-507. [Crossref]
- Liao HK, Gu Y, Diaz A, Marlett J, Takahashi Y, et al. (2015) Use of the CRISPR/Cas9 system as an intracellular defense against HIV-1 infection in human cells. Nat Commun 6: 6413. [Crossref]
- Zhu W, Lei R, Le Duff Y, Li J, Guo F, et al. (2015) The CRISPR/Cas9 system inactivates latent HIV-1 proviral DNA. Retrovirology 12: 22. [Crossref]
- Kaminski R, Chen Y, Salkind J, Bella R, Young WB, et al. (2016) Negative Feedback Regulation of HIV-1 by Gene Editing Strategy. Sci Rep 6: 31527. [Crossref]
- Kaminski R, Bella R, Yin C, Otte J, Ferrante P, et al. (2016) Excision of HIV-1 DNA by gene editing: a proof-of-concept in vivo study. Gene Ther 23: 690-695.
- Yin C, Zhang T, Qu X, Zhang Y, Putatunda R, et al. (2017) In Vivo Excision of HIV-1 Provirus by saCas9 and Multiplex Single-Guide RNAs in Animal Models. Mol Ther 25: 1168-1186. [Crossref]
- Huang Z, Nair M (2017) A CRISPR/Cas9 guidance RNA screen platform for HIV provirus disruption and HIV/AIDS gene therapy in astrocytes. Sci Rep 7: 5955. [Crossref]
- Kunze C, Börner K, Kienle E (2018) Synthetic AAV/CRISPR vectors for blocking HIV-1 expression in persistently infected astrocytes. Glia 66: 413-427. [Crossref]
- Dampier W, Sullivan NT (2017) Designing broad-spectrum anti-HIV-1 gRNAs to target patient-derived variants. Sci Rep 7: 14413. [Crossref]
- Dufour C, Claudel A, Joubarne N, Merindol N, Maisonnet T, et al. (2018) Editing of the human TRIM5 gene to introduce mutations with the potential to inhibit HIV-1. PLoS One 13: e0191709. [Crossref]
- Taylor JP, Cash MN, Santostefano KE, Nakanishi M (2018) CRISPR/Cas9 knockout of USP18 enhances type I IFN responsiveness and restricts HIV-1 infection in macrophages. J Leukoc Biol. [Crossref]
- Wang Z, Pan Q, Gendron P, Zhu W, Guo F, et al. (2016) CRISPR/Cas9-Derived Mutations Both Inhibit HIV-1 Replication and Accelerate Viral Escape. Cell Rep 15: 481-489. [Crossref]
- Wang G, Zhao N, Berkhout B, Das AT (2016) CRISPR-Cas9 Can Inhibit HIV-1 Replication but NHEJ Repair Facilitates Virus Escape. Mol Ther 24: 522-526. [Crossref]
- Ueda S, Ebina H, Kanemura Y, Misawa N, Koyanagi Y (2016) Anti-HIV-1 potency of the CRISPR/Cas9 system insufficient to fully inhibit viral replication. Microbiol Immunol 60: 483-496.
- Herrera-Carrillo E, Berkhout B (2016) Attacking HIV-1 RNA versus DNA by sequence-specific approaches: RNAi versus CRISPR-Cas. Biochem Soc Trans 44: 1355-1365. [Crossref]
- Yoder KE, Bundschuh R (2016) Host Double Strand Break Repair Generates HIV-1 Strains Resistant to CRISPR/Cas9. Sci Rep 6: 29530. [Crossref]
- Wang G, Zhao N, Berkhout B, Das AT (2016) A Combinatorial CRISPR-Cas9 Attack on HIV-1 DNA Extinguishes All Infectious Provirus in Infected T Cell Cultures. Cell Rep 17: 2819-2826. [Crossref]
- Lebbink RJ, de Jong DC, Wolters F, Kruse EM, van Ham PM, et al. (2017) A combinational CRISPR/Cas9 gene-editing approach can halt HIV replication and prevent viral escape. Sci Rep 7: 41968. [Crossref]
- Zhao N, Wang G, Das AT, Berkhout B (2017) Combinatorial CRISPR-Cas9 and RNA Interference Attack on HIV-1 DNA and RNA Can Lead to Cross-Resistance. Antimicrob Agents Chemother 61: e01486- e015117.
- Schiffer JT, Swan DA, Stone D, Jerome KR (2013) Predictors of hepatitis B cure using gene therapy to deliver DNA cleavage enzymes: a mathematical modeling approach. PLoS Comput Biol 9: e1003131. [Crossref]
- Zhen S, Hua L, Takahashi Y, Narita S, Liu YH, et al. (2014) In vitro and in vivo growth suppression of human papillomavirus 16-positive cervical cancer cells by CRISPR/Cas9. Biochem Biophys Res Commun 450: 1422-1426.
- White MK, Hu W, Khalili K (2015) The CRISPR/Cas9 genome editing methodology as a weapon against human viruses. Discov Med 19: 255-262.
- Wollebo HS, Bellizzi A, Kaminski R, Hu W, White MK, et al. (2015) CRISPR/Cas9 System as an Agent for Eliminating Polyomavirus JC Infection. PLoS One 10: e0136046. [Crossref]
- Bogerd HP, Kornepati AV, Marshall JB, Kennedy EM, Cullen BR (2015) Specific induction of endogenous viral restriction factors using CRISPR/Cas-derived transcriptional activators. Proc Natl Acad Sci USA 112: E7249-E7256.
- Choi JG, Dang Y, Abraham S, Ma H, Zhang J, et al. (2016) Lentivirus pre-packed with Cas9 protein for safer gene editing. Gene Ther 23: 627-633. [Crossref]
- Wahid B, Usman S, Ali A, Saleem K, Rafique S, et al. (2017) Therapeutic Strategies of Clustered Regularly Interspaced Palindromic Repeats-Cas Systems for Different Viral Infections. Viral Immunol 30: 552-559.
- Roesch F, OhAinle M, Emerman M (2018) A CRISPR screen for factors regulating SAMHD1 degradation identifies IFITMs as potent inhibitors of lentiviral particle delivery. Retrovirology 15: 26.
- Wu HY, Cao CY (2018) The application of CRISPR-Cas9 genome editing tool in cancer immunotherapy. Brief Funct Genomics.
- Wang C, Jin H, Gao D, Wang L, Evers B, et al. (2018) A CRISPR screen identifies CDK7 as a therapeutic target in hepatocellular carcinoma. Cell Res.
- Wang G, Chow RD, Ye L, Guzman CD, Dai X, et al. (2018) Mapping a functional cancer genome atlas of tumor suppressors in mouse liver using AAV-CRISPR-mediated direct in vivo screening. Sci Adv 4: eaao5508.
- Chira S, Gulei D, Hajitou A, Berindan-Neagoe I (2018) Restoring the p53 ‘Guardian’ Phenotype in p53-Deficient Tumor Cells with CRISPR/Cas9. Trends Biotechnol 18: 30048-30049.
- Norouzi-Barough L, Sarookhani M, Salehi R, Sharifi M, Moghbelinejad S (2018) CRISPR/Cas9, a new approach to successful knockdown of ABCB1/P-glycoprotein and reversal of chemosensitivity in human epithelial ovarian cancer cell line. Iran J Basic Med Sci 21: 181-187.
- Cradick TJ, Fine EJ, Antico CJ, Bao G (2013) CRISPR/Cas9 systems targeting β-globin and CCR5 genes have substantial off-target activity. Nucleic Acids Res 41: 9584-9592. [Crossref]
- Sakurai T, Watanabe S, Kamiyoshi A, Sato M, Shindo T (2014) A single blastocyst assay optimized for detecting CRISPR/Cas9 system-induced indel mutations in mice. BMC Biotechnol 14: 69.
- Ding Q, Strong A, Patel KM, Ng SL, Gosis BS, et al. (2014) Permanent alteration of PCSK9 with in vivo CRISPR-Cas9 genome editing. Circ Res 115: 488-492. [Crossref]
- Nakamura K, Fujii W, Tsuboi M, Tanihata J, Teramoto N, et al. (2014) Generation of muscular dystrophy model rats with a CRISPR/Cas system. Sci Rep 4: 5635. [Crossref]
Horii T, Arai Y, Yamazaki M, Morita S, Kimura M, et al. (2014) Validation of microinjection methods for generating knockout mice by CRISPR/Cas-mediated genome engineering. Sci Rep 4: 4513.


