Автор: Росица Ташкова
Биохимичен състав и структура на пептидогликана
Пептидогликанът (муреин) е основен, специфичен компонент на бактериалната клетъчна стена. Основната му функция е да запазва целостта на клетката, като противостои на тургорното налягане. Инхибирането на биосинтезата му (чрез мутация, под действието на антибиотици) или специфичното му разграждане (например от лизозим) по време на клетъчния растеж, води до лизис на клетката. Пептидогликанът е важен и за поддържане на определена форма на клетката и служи като основа за прикрепване на различни други компоненти, например белтъци (Dramsi et al., 2008) и тейхоеви киселини (при Грам положителните бактерии) (Neuhaus & Baddiley, 2003). Той е тясно свързан с процесите на клетъчен растеж и делене. Някои бактериални видове не притежават пептидогликан – Mycoplasma, Planctomyces и Orientia (Rickettsia) tsutsugamushi (Moulder, 1993; Tamura et al., 1995). Никога не е бил наблюдаван и при Chlamidia sp., въпреки че те притежават повечето от гените, необходими за биосинтезата му (Chopra et al., 1998; Ghuysen & Goffin, 1999).
Основните структурни компоненти на пептидогликана са линейни гликанови вериги, омрежени от къси пептиди. Гликановите вериги са съставени от редуващи се N-ацетилглюкозамин и N-ацетилмурамова киселина, свързани чрез β-(1-4) връзки. D-лактоиловата група на всеки остатък N-ацетилмурамова киселина е заместена с пептидна верига, която най-често има следната структура: L-Ala-γ-D-Glu-мезо-A2pm (или L-Lys) -D-Ala-D-Ala (A2pm е 2,6-диаминопимелинова киселина), като при зреене на макромолекулата, последният D-аланинов остатък се губи (Vollmer et al., 2008). Омрежването на гликановите вериги обикновено възниква между карбоксилната група на D-аланина на четвърта позиция и аминогрупата на диаминопимелиновата киселина на трета позиция, или директно, или чрез къс интерпептиден мост. Така, химическата характеристика на този хетерополимер включва присъствието на необичайния въглехидрат N-ацетилмурамова киселина, γ-свързана D-глутаминова киселина, L-D (или дори D-D) връзки и небелтъчни аминокиселини (A2pm) (Vollmer et al., 2008).
Гореописаната структура на пептидогликана се запазва при всички известни бактериални видове. Въпреки това, съществуват известни вариации между видовете – главно в пептидната верига, гликановите вериги или в местоположението или състава на интерпептидния мост. Може да съществуват и вътревидови вариации във фината структура на пептидогликана, зависещи от условията на растеж (фаза на растеж, състав на хранителната среда, наличие на антибиотици) (Vollmer et al., 2008).
Особености в структурата на пептидогликана на Staphylococcus aureus
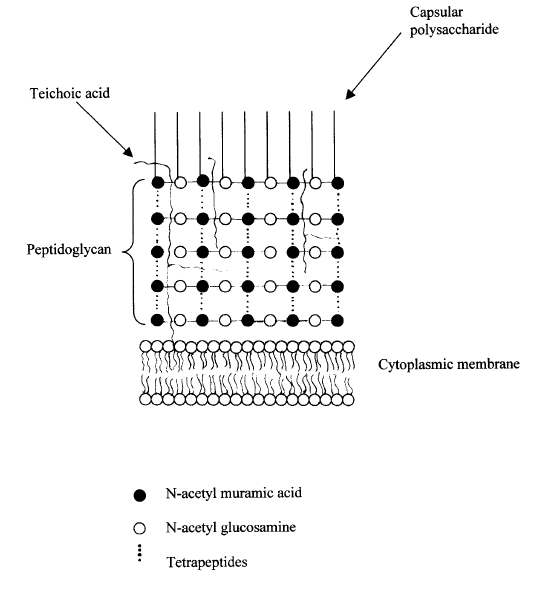
Пептидогликанът на Staphylococcus aureus представлява хетерогенен, силно омрежен полимер, което го прави особено труден за разрушаване. Дебелината му е около 20-30 nm. Пептидните вериги при S. aureus имат следната структура: L-аланин-D-изо-глутамин-L-лизин-D-аланин-D-аланин, а интерпептидният мост е пентаглицинов сегмент (Фиг. 1 и 2).


Последните стъпки от изграждането на пептидогликана включват участието на два много важни ензима – трансгликозилаза (Labischinski, 1992) и транспептидаза (de Lencastre et al., 1994), разположени отвъншната страна на цитоплазматичната мембрана. Трансгликозилазата катализира формирането на β-(1–4) гликозидна връзка между дизахаридите на гликановите единици, които формират полимера на основната гликанова верига. Новоформираната гликанова верига, често наричана насцентен пептидогликан, се вгражда в клетъчната стена от транспептидазата. Транспептидазата медиира омрежването чрез създаване на пептидна връзка между N-края на последния глицинов остатък от пентаглициновия сегмент, прикачен към една от пептидните вериги, и D-аланина на четвърто място, който е част от съседна пептидна верига (van Heijenoort, 2001). Резултатът от активностите на трансгликозилазата и транспептидазата е формирането на пептидогликанова мрежа, която обхваща цялата клетка (Sharif et al., 2009).
Биохимична структура на тейхоевите киселини при Staphylococcus aureus
Тейхоевите киселини са значима част от клетъчната стена на Staphylococcus aureus. Повечето щамове експресират полирибитолфосфатни тейхоеви киселини, заместени с D-аланин и N-ацетилглюкозаимн (Xia & Peschel, 2008). Модификациите в захарните остатъци на тейхоевите киселини силно варират. Staphylococcus aureus и повечето Грам-положителни бактерии експресират на повърхността си тейхоеви киселини, които са свързани или с мембранни липиди (липотейхоеви киселини), или с N-ацетилмурамовата киселина от пептидогликана на клетъчната стена (Фиг. 3). Последните са съставени от повтарящи се единици, които съдържат фосфат и са с много вариабилен и често видовоспецифичен състав. Полирибитолфосфатните тейхоеви киселини са изградени от повтарящи се единици D-рибитол, свързани чрез 1,5-фосфодиестерни връзки.
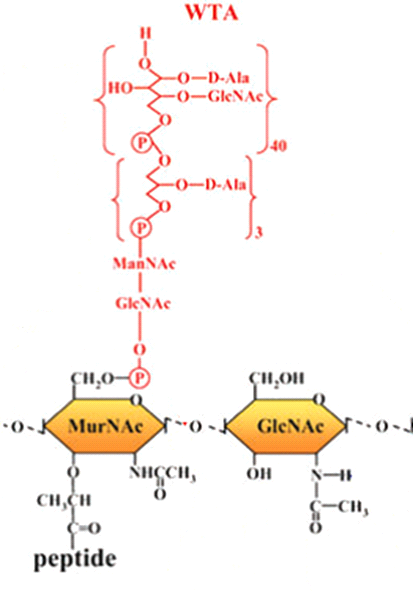
Тейхоевите киселини са ковалентно свързани с пептидогликана чрез линкерна единица, която обикновено представлява N-ацетилглюкозамин-N-ацетилманозаминов дизахарид. При S. aureus полимерът съдържа 2 или 3 глицеролфосфатни единици, последвани от около 40 рибитолфосфатни, които може допълнително да бъдат модифицирани с N-ацетилглюкозамин и D-аланин (Фиг. 4) (Xia & Peschel, 2008).
Стафилолитични ензими
Някои патогенни бактерии се характеризират с естествена резистентност към бактерицидните компоненти на тъканите на гостоприемника. Това обикновено се дължи на структурни особености. Например, присъствието на D-аланин в тейхоевите киселини на Staphylococcus aureus (Peschel et al., 1999) определя устойчивостта на бактерията към дефензините, протегрините и други антимикробни пептиди. Освен това, S. aureus притежава допълнително структурни или биохимични особености, които му позволяват да устоява на защитните механизми на гостоприемника. Телесните течности и тъканите на животните съдържат разнообразие от антимикробни вещества, които убиват или потискат растежа на бактериите. Те се наричат тъканни бактерициди (Bera et al., 2005).
Един от най-важните и широкоразпространени тъканни бактерициди е лизозимът. Той е мурамидаза, която разгражда пептидогликана чрез разкъсване на гликозидната β-(1-4) връзка между N-ацетилмурамовата киселина и N-ацетилглюкозамина. Произвежда се от различни тъкани (мукозни мембрани, респираторен и храносмилателен тракт) и се открива в телесни течности като слюнка, серум, пот и сълзи. Титърът му се повишава при инфекция и се индуцира синтезът му в различни клетки (моноцити, макрофаги) (Keshav et al., 1991).
Без съмнение лизозимът е много важен защитен компонент, но патогенните бактерии, които колонизират гостоприемника за дълъг период от време или причиняват хронични инфекции, са развили механизми, които да неутрализират действието му.
Staphylococcus aureus е напълно нечувствителен към лизозима, което допринася много за устойчивостта и успешното колонизиране на кожата и лигавиците при човека и животните. Точният механизъм на тази устойчивост все още не напълно изяснен, но се обсъждат различни предположения: O-ацетилирането на N-ацетилмурамовата киселина в пептидогликана (Bera et al., 2005), прикрепването на други полимери (например полизахариди) към клетъчната стена, високата степен на омрежване на пептидогликана и незаместените остатъци N-глюкозамин, както е при Bacillus cereus и Streptococcus pneumonia (Vollmer and Tomasz, 2000).
Ензимите, хидролизиращи пептидогликана на S. aureus представляват алтернатива на антибиотиците, въпреки опасността от развиване на резистентност, имуногенност и освобождаването на компоненти от лизиралите клетки, които могат да предизвикат възпаление. В следващите точки ще бъдат разгледани няколко ензима, които притежават способността да разграждат клетъчната стена на Staphylococcus aureus.
- Автолизин Atl
Автолизините са бактериолитични ензими, които разграждат пептидогликана на бактериите, които ги продуцират. Въпреки че са потенциално опасни за клетката, те са широкоразпространени сред бактериите, които притежават пептидогликан (Smith et al., 2000).
Муреин хидролазите са хидролитични ензими, участващи в деградацията, обмяната и зреенето на бактериалния пептидогликан. Те играят съществена роля в клетъчното делене чрез осигуряването на точно разделяне на клетка. Поради тяхната активност, те са строго регулирани, за да се предотврати внезапен лизис – това е феноменът, който дава името им. Най-важната муреин хидролаза на S. aureus е AtlA, която се експресира като про-протеин с дължина 1 257 аминокиселини (137,5 kDa). Той претърпява протеолитично срязване до сигнална секвенция с размер 3,1 kDa, 17,6 kDa пропептид с неизвестна функция и два каталитично активни протеина – AM и GL (Oshida et al., 1995). AM (63,3 kDa) е N-ацетилмурамил-L-аланин амидаза, която къса амидната връзка между N-ацетилмурамовата киселина в муреиновия скелет и L-аланина в пептидната верига (Biswas et al., 2006). В допълнение, AM притежава един ензимен домен и два повторени домена, които участват в локализацията и субстратното разпознаване (Biswas et al., 2006; Baba & Schneewind, 1998). GL (53,6 kDa) е ендо-β-N-ацетилглюкозаминидаза, която хидролизира връзката между N-ацетил -β-D-глюкозамина и N-ацетилмурамовата киселина и съдържа ензимен домен и един повторен домен (Oshida et al., 1995). Кталитичния домен на GL без повтора е с размер около 36 kDa (Bose et al., 2012).
Предполага се, че в отсъствие на Atl, други муреин хидролази могат поне отчасти да компенсират загубата на активността му. Възможни компенсиращи муреин хидролази са Sle1 (Kajimura et al., 2005), LytN (Frankel et al., 2011), LytM (Ramadurai & Jayaswal, 1997), както и повече от 15 други протеина с предполагаема амидазна и глюкозаминидазна активност (Frankel et al., 2011; Delaune et al., 2011).
- Лизостафин
Лизостафинът е мономерен цинков металоензим с дължина 246 аминокиселини. Молекулната му маса е около 27 kDa, изоелектричната му точка е 9,5, а pH-оптимумът – 7,5 (Browder et al., 1965; Trayer & Buckley, 1970). Той е бактериоцин, произвеждан от Staphylococcus simulans биовар staphylolyticus. Синтезира се като препроензим с дължина 493 аминокиселини и притежава N-краен лидерен пептид от 36 аминокиселини (Фиг. 5). Проензимът се освобождава в културалната среда и съдържа 15 тандемни повтора по 13 аминокиселини в N-края си (Heinrich et al., 1987). Пролизостафинът е 4,5 пъти по-слабо активен преди зреене на ензима, което се осъществява чрез секретиране на цистеинова протеаза по време на растежната фаза, отстраняваща N-крайните повтори (Thumm & Götz, 1997). Молекулата на лизостафина се състои от два различни домена: N-краен пептидазен домен, отговорен за каталитичното действие на протеина (Schindler & Schudhardt, 1964) и C-краен насочващ домен, който участва в свързването а пептидогликана като субстрат (Simmonds et al., 1997; Baba & Schneewindt, 1996). C-крайният домен е с дължина 92 аминокиселини и не е задължителен за ензимната активност на лизостафина, но е необходим за насочването му към клетъчната стена на S. aureus. Мутантен лизостафин без насочващ домен губи способността си да се свързва със стафилококите и да разграничава таргетните клетки (Baba & Schneewind, 1996). Такъв домен се открива и при други видове пептидогликан хидролази, например С-краят на N-ацетилмурамил-L-аланин амидазата и N-краят на глюкозаминидазата, които са продукт на стафилококовия автолизин Atl. Тези домени насочват автолизина към екваториалната повърхност на S. aureus (Lu et al., 2006).
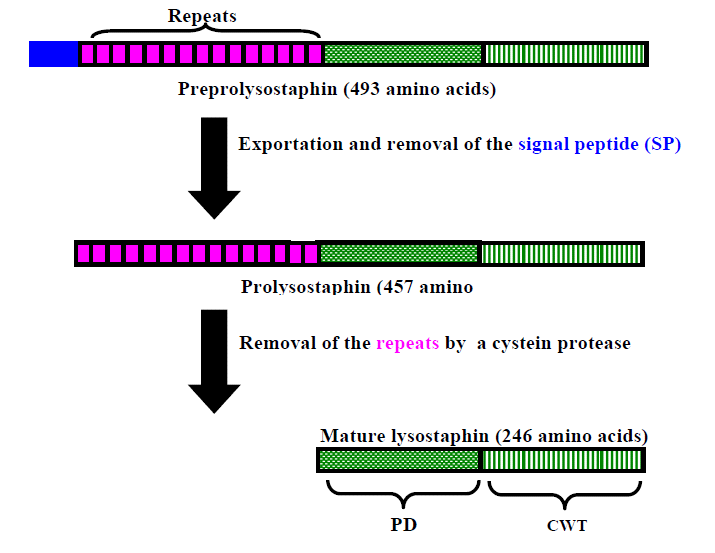
- simulans произвежда лизостафин по време на стационарната фаза и при определени условия това е координирано с продукцията на други извънклетъчни ензими (Larrimore et al., 1982). Продуцентите на лизостафин не притежават специфични имунни гени, а разчитат на резистентност, за да оцелеят по време на биосинтезата на този ензим. Генът за ендопептидазния домен на лизостафина lss и генът, отговорен за резистентност към лизостафин lif се разполагат върху плазмида pACK1 (Thumm & Götz, 1997; Heath et al., 1987; Heath et al., 1989). Двата гена са фланкирани от инсерционни секвенции, което предполага, че S. simulans биовар staphylolyticus може да е получил тези гени чрез хоризонтален трансфер (Thumm & Götz, 1997).
Лизостафинът свободно преминава през капсулния слой на капсулираните стафилококи (King et al., 1980) и разрушава клетъчната стена на много щамове на Staphylococcus sp., действайки като глицил-глицинова ендопептидаза (Schindler & Schudhardt, 1965).
Поради способността на ензима да убива патогенни за човека стафилококи, като S. aureus и S. epidermidis, различни публикации от 60-те и 70-те години препоръчват употребата му срещу инфекции, причинени от тези патогени. Въпреки това, изучаването на лизостафина като средство за лечение е спряло поради наличието на други ефективни препарати. Но с бързото намаляване на активността на антибиотиците и възможността за синтез на рекомбинантен лизостафин, проучванията на лизостафина като терапевтичен агент срещу стафилококови инфекции, отново започват да се провеждат.
Лизостафинът притежава много добри характеристики като антибактериален агент: активен е както срещу делящи се, така и срещу неделящи се клетки, разгражда се от чревните протеази без да влияе на естествената микрофлора, не е токсичен, относително стабилен, когато е конюгиран с полиетиленгликол и запазва активността си в човешки серум (Williamson et al., 1994; Schaffner et al., 1967; Walsh et al., 2002). Освен това, според някои проучвания лизостафинът остава активен in vivo, без да предизвиква нежелана имунна реакция, освен повишаването на титъра на антитела срещу него (Zygmunt et al., 1972; Dajcs et al., 2002).
Употребата на комбинации от антимикробни агенти е обичайна, тъй като това разширява спектъра от засегнати бактерии; предотвратява възникването на резистентност; понижава токсичността, тъй като комбинацията позволява по-ниска концентрация на отделните компоненти; агентите може да действат синергистично. Синергия е наблюдавана in vitro между лизостафин и мембранно-активни агенти, като полимиксини В (Polak et al., 1993) и раналексин (Graham et al., 2007), който е катионен пептид, продуциран от жаби от рода Rana и е активен срещу MRSA.
Повишената употреба на интраваскуларни катетри за диагностика на заболявания и за терапевтични процедури, води до повишаване честотата на инфекции, свързани с тези медицински приспособления (Casey et al., 2007). Днес има много случаи на сепсис, възникнал поради колонизация на вътрешните повърхности на венозни катетри (Rogers et al., 2009; Harbarth et al., 2003). Лизостафинът е изследван като агент за превенция на повърхностна колонизация от S. aureus и S. epidermidis. Wu и сътр. (Wu et al., 2003) съобщават, че лизостафинът не просто убива S. aureus в биофилмите, но също разрушава екстрацелуларния матрикс на тези биофилми in vitro, върху пластмасови и стъклени повърхности и в ниски концентрации (1 μg/ml). За постигане на същия ефект при биофилмите на S. epidermidis са били необходими по-високи концентрации. В друго проучване, Shah и сътр. (Shah et al., 2004) изследвали ефективността на лизостафина, като покритие на два типа повърхности – полистиренови плаки и флуороетиленпропиленови катетри, инокулирани със S. aureus след като са били покрити с лизостафин. Полистиреновите плаки показали намаляване броя на бактериите с 99,5%, а катетрите останали напълно чисти. Инхибиторният ефект на покритието се запазил за не по-малко от четири дни.
Тези две проучвания показват, че лизостафинът се свързва с пластмасови повърхности, поддържайки антибактериална активност срещу стафилококите и може да предпазва катетрите от колонизация по време на употребата им и няколко дни след това.
2.1. Приложения на лизостафина in vivo
В литературата има добре описани експериментални приложения на лизостафина in vivo. Първото съобщение за ефективността на лизостафина срещу S. aureus in vivo е публикувано от Schuhardt и Schindler през 1964 (Schuhardt & Schindler, 1964). Те еднократно инжектирали частично пречистен лизостафин интраперитонеално или подкожно на заразени със S. aureus мишки и определили условна концентрация лизостафин (10 условни единици), която е достатъчна за оздравяването на всички мишки, независимо от начина на инжектиране.
Dixon и сътр. (Dixon et al., 1968) са изследвали ефективността на третиране с лизостафин (5 mg) и последващо третиране с метицилин (5 mg) срещу ренален абсцес при мишки. Приложението на еднократна доза лизостафин, последвано от четири ежедневни дози метицилин, довело до пълно елиминиране на стафилококовите популации. Приложението на двата агента поотделно не води до такива резултати. Аналогично, лечението на ендокардит, причинен от клинични изолати на MRSA (Climo et al., 1998) или щамове с понижена чувствителност към ванкомицин (VISA) (Patron & Climo, 1999) при зайци, е много по-ефективно при използване на комбинация от лизостафин и ванкомицин, отколкото при използване на веществата поотделно. Според изследването на Climo и сътр., в продължение на девет седмици след интравенозно инжектиране с рекомбинантен лизостафин не е настъпила имунологична реакция.
Kiri и сътр. (Kiri et al., 2002) съобщават, че лечението на зайци, заразени с метицилин-резистентен S. epidermidis с комбинация от нафцилин (200 mg/kg мускулно) и рекомбинантен лизостафин (1mg/kg интравенозно) показва много голяма ефективност и демонстрира синергията между рекомбинантния лизостафин и β-лактамните антибиотици – явление, което вече е описано при изследвания с MRSA (Climo et al., 2001).
Walsh и сътр. (Walsh et al., 2002) използват като модел мишки, за да сравнят фармакокинетиката на рекомбинантия лизостафин с тази на лизостафин, конюгиран с полиетиленгликол. Те са установили, че 24 часа след еднократна доза от 40 mg/kg рекомбинантен лизостафин, концентрацията му в серума спада 500 пъти, докато концентрацията на конюгата се понижава едва 10 пъти. Това показва повишената стабилност на лизостафина, благодарение на конюгацията с полиетиленгликол, което позволява намаляване на дозата и честотата на въвеждане на веществото в организма, необходими за поддържане на плазмените му концентрации над терапевтично ефективните. Поддържането на такива високи нива на рекомбинантен лизостафин може да спомогне за по-бързото отстраняване на бактериалната инфекция и понижаване на опасността от възникване на резистентност към ензима.
2.2. Резистентност към лизостафин
Клиничното приложение на лизостафин може да бъде ограничено от развитието на резистентност, както при много други антибактериални агенти. Не са открити резистентни към него мутанти при изследвания, проведени in vivo, в които са използвани високи дози лизостафин (Patron & Climo, 1999; Shah et al., 2004). Въпреки това, развитие на резистентност към лизостафин от S. aureus е съобщено от Strandén и сътр. (Strandén et al., 2003). Механизмът, който е отговорен за това изглежда може да бъде различен, но най-често срещаният включва мутации, които засягат или гена femA, или femB. Тези мутации се изразяват в скъсяване на пентаглициновия мост в пептидогликана до моно- или триглицинов (Ehlert et al., 1997; Strandén et al., 2003).
Climo и сътр. (Climo et al., 2001) са установили, че може да се появи резистентност към лизостафин както in vitro, така и при in vivo модел на инфекция с MRSA, в резултат от дълготрайно излагане на ниски концентрации лизостафин. Резистентността при такива мутанти е била свързана с три характеристики: повишена чувствителност към β-лактамни антибиотици, мутации в гена femA и изменена структура на пептидогликана, в която пентаглициновия мост е заменен само с един глицинов остатък. Освен това, комбинацията от лизостафин и β-лактамни антибиотици е синергична. Тези данни предполагат, че лизостафинът би трябвало да се използва заедно с β-лактамите за постигане на двоен ефект – потискане на резистентността и промотиране на синергията (Bastos et al., 2010).
Други изследвания също описват взаимоотношението между резистентността към лизостафин, породена от мутации във femA и повишената чувствителност към β-лактамните антибиотици (Kiri et al., 2002; Strandén et al., 2003). Демонстрирано е, че модифицираният пеницилин-свързващ белтък 2, кодиран от гена mecA и обуславящ резистентност към β-лактамните антибиотици при MRSA, не може да изпълнява своята функция в отсъствие на пентаглицинови интерпептидни мостове (Rohrer & Berger-Bächi, 2003). Същевременно, нормалният пеницилин-свързващ пептид 2 (PBP 2) може да използва тези моноглицинови мостове, но тъй като β-лактамните антибиотици могат да инхибират PBP 2, резултантният фенотип е чувствителен към метицилина (Guignard et al., 2005).
Morikawa и сътр. (Morikawa et al., 2001) установяват, че дебелината на клетъчната стена също има голямо значение за чувствителността към лизостафина. Те са използвали мутанти по гена sigB на S. aureus щам N315. Клетки с понижени нива на sigB синтезират по-тънки клетъчни стени и показват с 97% по-висока чувствителност към лизостафин в сравнение с дивия тип. Свръхпродукцията на sigB води до повишаване на резитентността към ензима с 300%. Повишената резистентност на тези клетки се отдава на значително удебеляване на клетъчната стена и в литературата се откриват данни в подкрепа на това твърдение. Например, ванкомицин-резистентният щам на S. aureus MU50 също притежава удебелена клетъчна стена, което се свързва с неговата резистентност към ванкомицин (Cui et al., 2000). Друго изследване (Koehl et al., 2004), изучаващо ниската чувствителност на VISA към лизостафин, показва, че освен с уголемената клетъчна стена, резистентността към лизостафин е свързана и с понижена автолитична активност на клетките. Предполага се, че при цели клетки автолизините участват в лизиса, наблюдаван след третиране с лизостафин и че нарушената автолиза при VISA е основната причина за слабата чувствителност на клетките им към лизостафин. При S. aureus са представени няколко гена за автолизини. Аtl е генът, който кодира основния автолизин на този бактериален вид. Той търпи постранслационен процесинг до амидаза с размер 63 kDa и глюкозаминидаза с размер 53,5 kDa. Експресията на atl при VISA е значително намалена, което потвърждава допускането, че именно автолизините са отговорни за възникването на лизис след третиране с лизостафин (Bastos et al., 2010).
Gründling и сътр. (Gründling et al., 2006) са идентифицирали друг ген в S. aureus – lyrA, чиято инактивация води до високи нива на лизостафинова резистентност. Този ген кодира полипептид с дължина 419 аминокиселини и неизвестна функция.
Въпреки тези съобщения за възникване на разистентност към лизостафина, много важно наблюдение е направено от Kusuma и сътр. (Kusuma et al., 2007), които демонстрират, че развитието на резистентност, дължаща се на мутация в гена femA при два щама MRSA, също води и до загуба на жизнеспособност, което се изразява в намален растеж по време на логаритмичната фаза, повишена чувствителност към високи температури и поне пет пъти по-слаба вирулентност на мутантите в сравнение с дивия тип при мишки. За период от 14 дни на серийни препосявания и без селективен натиск, мутантите не са развили компенсаторни мутации, които да възстановят жизнеспособността им (Bastos et al., 2010).
В заключение, тези резултати показват, че ако възникне резистентност, поради изменение функцията на FemA при S. aureus, резистентните варианти ще бъдат с потисната жизненост и вирулентност, като в допълнение инфекциите с тези щамове ще бъдат лечими с β-лактамни антибиотици (Kokai-Kun et al., 2009).
- ALE-1
ALE-1 е близък хомолог на лизостафина и се продуцира от Staphylococcus capitis EPK1 (Sugai et al., 1997). Той притежава модулна структура, близка до тази на лизостафина. Изграден е от N-краен повтор от 13 аминокиселини, последван от централен каталитичен домен и C-краен насочващ домен от 92 аминокиселини, който е изключително близък до този на лизостафина. За разлика от него обаче, ALE-1 не претърпява пост-транслационен процесинг на N-крайния повтор (Lu et al., 2006).
- LytM
LytM е автолизин на Staphylococcus aureus под контрола на двукомпонентата система WalKR, за която се смята, че играе роля във вирулентността и метаболизма на клетъчната стена (Dubrac & Msadek, 2004). Белтъкът се синтезира със сигнален пептид, последван от N-краен домен, който е хомолог на стафилококовия секреторен антиген А – друг протеин, контролиран от WalKR, но не е хомолог на N-крайния домен на лизостафина. C-крайният домен на LytM може да бъде подразделен на оклузиращ регион и регион с голямо сходство с каталитичния домен на лизостафина. Аминокиселинните остатъци в активния център са като тези на лизостафина с централен цинков катион, координиран от His210, Asp214 и His293 на каталитичния домен (Odintsov et al., 2004). Въпреки това, структурата предполага, че LytM в пълната си дължина не може да притежава висока активност, защото активният център е оклудиран (Odintsov et al., 2004). Но според кристалната структура, каталитичният домен би трябвало да бъде по-активен сам, отколкото протеинът в неговата цялост (Odintsov et al., 2004; Firczuk et al., 2005). LytM не притежава аналог на насочващия домен на лизостафина.
Биологичната роля на LytM все още не е ясна (Singh et al., 2010). Белтъкът първоначално е описан като автолизин (Mani et al., 1995) с глицил-глицинова ендопептидазна активност (Ramadurai & Jayaswal, 1997). Изледвания, проведени по-късно, хвърлят съмнение върху пептидогликан хидролизиращата активност на ензима в пълната му дължина (Odintsov et al., 2004; Singh et al., 2010). Въпреки това, данните ясно потвърждават, че каталитичният фрагмент има такава активност (Odintsov et al., 2004; Firczuk et al., 2005). Трябва да бъде потвърдено дали каталитичният домен на LytM може да бъде освобождаван при физиологични условия. Протеомно изследване на фракция от клетъчната стена на S. aureus е установило наличие на LytM само в неговата пълна дължина (с молекулна маса около 40 kDa и изоелектрична точка около 6), но не и в очакваната активна форма (Pieper et al., 2006). Въпреки че физиологичната роля на LytM и неговия каталитичен домен остава неясна, каталитичният домен има свойства, които може да го направят потенциален агент за лечение на стафилококови инфекции. Протеинът може да бъде свръхекспресиран в Escherichia coli в много високи нива и е лесен за пречистване (Firczuk et al., 2005).
Докато нативният LytM притежава незначителен бактерициден ефект, сливането му с насочващия домен на лизостафина повишава антистафилококовата му активност около 540 пъти, което го нарежда сред много фагови лизини, които се намират в процес на предклинични изпитания (Bastos et al., 2010). Възможността ендогенната система на патогените за рециклиране на пептидогликана да бъде подчинена на терапевтични цели ни отваря врати към резервоар от потенциални антибактериални агенти, които не са били проучени досега (Osipovitch & Griswold, 2015).
- Стафилолитични ензими, продуцирани от Aeromonas sp.
През 1969 г. Coles и сътр. изолират и характеризират ензим, продуциран от Aeromonas hydrophila, който е способен да лизира клетките на Staphylococcus aureus. Ензимът е пречистен чрез гел-филтрация и хроматография в колони с катионобменна смола AG-50 W (Bio-Rad®). Той е малък алкален протеин с нисък седиментационен коефициент и изоелектрична точка между pH 9,0 и pH 9,5. Максимална литична активност е постигната в 20 mM Трис-глицинов буфер при pH 8,5 и температура 45°С (Фиг. 6).
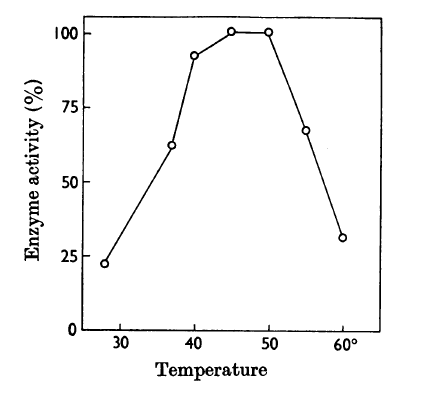
В отсъствие на азотни бази не е отчетено наличие на активност. Ензимът е активен в посочения буфер в присъствие на 1,5 М захароза и може да бъде използван за приготвянето на метаболитно активни протопласти на S. aureus (Coles & Gross, 1973). Авторите на изследването подлагат пептидогликана на два различни щама S. aureus на действието на ензима и в резултат се освобождават глицинови олигопептиди, основно диглицин и триглицин, което води до заключението, че ензимът разгражда пентаглициновия мост в пептидогликана на клетъчната стена (Coles et al., 1969).
През 1973 Wretlind и сътр. установяват, че стафилолитичният ензим се синтезира по време на логаритмичната фаза на растеж (Wretlind et al., 1973). Wretlind също допуска, че ензимът вероятно е локализиран в периплазматичното пространство на бактериалната клетка или активно се екскретира по време на растежа (Wretlind, непубликувани наблюдения). След това тази ензимна активност повече не е била обект на научен интерес.
Библиография:
- Baba T, Schneewindt O (1996) Target cell specificity of a bacteriocin molecule: a C-terminal signal directs lysostaphin to the cell wall of Staphylococcus aureus. EMBO J. 15: 4789–4797.
- Baba T, Schneewind O (1998) Targeting of muralytic enzymes to the cell division site of Gram-positive bacteria: repeat domains direct autolysin to the equatorial surface ring of Staphylococcus aureus. EMBO J. 17: 4639–4646.
- Bastos MCF, Coutinho BG and CoelhoMLV (2010) Lysostaphin: A Staphylococcal Bacteriolysin with Potential Clinical Applications. Pharmaceuticals. 3: 1139-1161.
- Bera A, Herbert S, Jakob A, Vollmer W and Götz F (2005) Why are pathogenic staphylococci so lysozyme resistant? The peptidoglycan O-acetyltransferase OatA is the major determinant for lysozyme resistance of Staphylococcus aureus. Molecular Microbiology. 55(3): 778–787
- Biswas R, Voggu L, Simon UK, Hentschel P, Thumm G, et al. (2006) Activity of the major staphylococcal autolysin Atl. FEMS Microbiology Letters. 259: 260–268.
- Bose JL, Lehman MK, Fey PD, Bayles KW (2012) Contribution of the Staphylococcus aureus Atl AM and GL murein hydrolase activities in cell division, autolysis, and biofilm formation. PLoS One. 7(7):e42244.
- Browder HP, Zygmunt WA, Young JR, Tavormina PA (1965) Lysostaphin: enzymatic mode of action. Biochem Biophys Res Commun. 19: 383–389.
- Casey AL, Lambert PA, Elliott TSJ (2007) Staphylococci. J Antimicrob Agents. 29 (Suppl. 3), S23–S32.
- Climo MW, Ehlert K, Archer GL (2001) Mechanism and suppression of lysostaphin resistance in oxacillin-resistant Staphylococcus aureus. Antimicrob Agents Chemother. 45: 1431–1437.
- Climo MW, Patron RL, Goldstein BP, Archer GL (1998) Lysostaphin treatment of experimental methicillin-resistant Staphylococcus aureus aortic valve endocarditis. Antimicrob Agents Chemother. 42: 1355–1360
- Coles NW, Gross R (1973) Preparation of Metabolically Active Staphylococcus aureus Protoplasts by Use of the Aeromonas hydrophila Lytic Enzyme; J Bact. 115(3): 746-751.
- Cui L, Murakami H, Kuwahara-Arai K, Hanaki H, Hiramatsu K (2000) Contribution of a thickened cell wall and its glutamine nonamidated component to the vancomycin resistance expressed by Staphylococcus aureus Mu50. Antimicrob Agents Chemother. 44: 2276–2285.
- Dajcs JJ, Thibodeaux BA, Girgis DO, Shaffer MD, Delvisco SM, O’Callaghan RJ (2002) Immunity to lysostaphin and its therapeutic value for ocular MRSA infections in the rabbit. Invest Opthalmol Visual Sci. 43: 3712–3716.
- de Lencastre H, de Jonge BLM, Matthews PR, and Tomasz A (1994) Molecular aspects of methicillin resistance in Staphylococcus aureus. J Antimicrob Chemother. 33: 7-14.
- Delaune A, Poupel O, Mallet A, Coic YM, Msadek T, et al. (2011) Peptidoglycan crosslinking relaxation plays an important role in Staphylococcus aureus WalKR-dependent cell viability. PLoS ONE. 6: e17054.
- Dixon RE, Goodman JS, Koenig MG (1968) Lysostaphin: an enzymatic approach to staphylococcal disease. III. Combined lysostaphin-methicillin therapy of established staphylococcal abscesses in mice. Yale J Biol Med. 41: 62–68
- Dramsi S, Davison S, Magnet S & Arthur M (2008) Surface proteins covalently attached to peptidoglycan: examples from both gram-positive and gram-negative bacteria. FEMS Microbiol Rev, in press.
- Dubrac S, Msadek T (2004) Identification of genes controlled by the essential YycG/YycF two-component system of Staphylococcus aureus. J Bacteriol. 186(4): 1175–1181.
- Ehlert K, Schrodr W, Labischinski H (1997) Specificities of FemA and FemB for different glycine residues: FemB cannot substitute for FemA in staphylococcal peptidoglycan pentaglycine side chain formation. J Bacteriol. 179: 7573–7576.
- Firczuk M, Mucha A, Bochtler M (2005) Crystal structures of active LytM. J Mol Biol. 354(3): 578–590.
- Frankel MB, Hendrickx AP, Missiakas DM, Schneewind O (2011) LytN, a Murein Hydrolase in the Cross-wall Compartment of Staphylococcus aureus, Is Involved in Proper Bacterial Growth and Envelope Assembly. J Biol Chem. 286: 32593–32605.
- Ghuysen JM & Goffin C (1999) Lack of cell wall peptidoglycan versus penicillin sensitivity: new insights into the chlamydial anomaly. Antimicrob Agents Chemother. 43: 2339–2344.
- Graham S, Coote PJ (2007) Potent, synergistic inhibition of Staphylococcus aureus upon exposure to a combination of the endopeptidase lysostaphin and the cationic peptide ranalexin. J Antimicrob Chemother. 59: 759–762.
- Gründling A, Missiakas DM, Schneewind O (2006) Staphylococcus aureus mutants with increased lysostaphin resistance. J Bacteriol. 188: 6286–6297.
- Guignard B, Entenza JM, Moreillon P (2005) Beta-lactams against methicillin-resistant Staphylococcus aureus. Curr Opin Pharmacol. 5: 479–489.
- Harbarth S, Sax H, Gastmeier P (2003) The preventable proportion of nosocomial infections: an overview of published reports. J Hosp Infect. 54: 258–266.
- Heinrich P, Rosenstein R, Bohmer M, Sonner P, Götz F (1987) The molecular organization of the lysostaphin gene and its sequences repeated in tandem. Mol Gen Genet. 209: 563–569.
- Kajimura J, Fujiwara T, Yamada S, Suzawa Y, Nishida T, et al. (2005) Identification and molecular characterization of an N-acetylmuramyl-L-alanine amidase Sle1 involved in cell separation of Staphylococcus aureus. Molecular Microbiology. 58: 1087–1101.
- Keshav S, Chung P, Milon G, and Gordon S (1991) Lysozyme is an inducible marker of macrophage activation in murine tissues as demonstrated by in situ hybridization. J Exp Med. 174: 1049–1058.
- King BF, Biel ML, Wilkinson BJ (1980) Facile penetration of the Staphylococcus aureus capsule by lysostaphin. Infect Immun. 29: 892–896.
- Kiri N, Archer G, Climo MW (2002) Combinations of lysostaphin with β-lactams are synergistic against oxacillin-resistant Staphylococcus epidermidis. Antimicrob Agents Chemother. 46: 2017–2020.
- Koehl JL, Muthaiyan A, Jayaswal RK, Ehlert K, Labischinski H, Wilkinson BJ (2004) Cell wall composition and decreased autolytic activity and lysostaphin susceptibility of glycopeptideintermediate Staphylococcus aureus. Antimicrob Agents Chemother. 48: 3749–3757.
- Kokai-Kun JF, Chanturiya T, Mond JJ (2009) Lysostaphin eradicates established Staphylococcus aureus biofilms in jugular vein catheterized mice. J Antimicrob Chemother. 64: 94–100.
- Kusuma CM, Jadanova A, Chanturiya T, Kokai-Kun JF (2007) Lysostaphin-resistant variants of Staphylococcus aureus demonstrate reduced fitness in vitro and in vivo. Antimicrob Agents Chemother. 51: 475–482.
- Labischinski H. (1992) Consequences of the interaction of beta-lactam antibiotics with penicillin binding proteins from sensitive and resistant Staphylococcus aureus strains. Med Microbiol Immunol. 181:241–265.
- Larrimore SA, Clark SB, Robinson JM, Heath HE, Sloan GL (1982) Coordinate production of three exoenzymes by Staphylococcus staphylolyticus. J Gen Microbiol. 128: 1529–1535.
- Lu JZ, Fujiwara T, Komatsuzawa H, Sugai M, Sakon J (2006) Cell wall-targeting domain of glycylglycine endopeptidase distinguishes among peptidoglycan cross-bridges. J Biol Chem. 281(1):549-58.
- Morikawa K, Maruyama A, Inose Y, Higashide M, Hayashi H, Ohta T (2001) Overexpression of sigma factor, sigma (B), urges Staphylococcus aureus to thicken the cell wall and to resist betalactams. Biochem Biophys Res Commun. 288: 385–389.
- Neuhaus FC & Baddiley J (2003) A continuum of anionic charge: structures and functions of d-alanyl-teichoic acids in gram-positive bacteria. Microbiol Mol Biol Rev. 67: 686–723.
- Odintsov SG, Sabala I, Marcyjaniak M, Bochtler M (2004) Latent LytM at 1.3A resolution. J Mol Biol. 335(3): 775–785.
- Oshida T, Sugai M, Komatsuzawa H, Hong YM, Suginaka H, et al. (1995) A Staphylococcus aureus autolysin that has an N-acetylmuramoyl-L-alanine amidase domain and an endo-beta-N-acetylglucosaminidase domain: cloning, sequence analysis, and characterization. Proceedings of the National Academy of Sciences of the USA. 92: 285–289.
- Osipovitch DC, Griswold KE (2015) Fusion with a cell wall binding domain renders autolysin LytM a potent anti-Staphylococcus aureus agent. FEMS Microbiol Lett. 362(2): 1-7.
- Patron RL, Climo MW, Goldstein BP, Archer GL (1999) Lysostaphin treatment of experimental aortic valve endocarditis caused by a Staphylococcus aureus isolate with reduced susceptibility to vancomycin. Antimicrob Agents Chemother. 43: 1754–1755.
- Peschel A, Otto M, Jack RW, Kalbacher H, Jung G, and Götz F (1999) Inactivation of the dlt operon in Staphylococcus aureus confers sensitivity to defensins, protegrins, and other antimicrobial peptides. J Biol Chem. 274: 8405–8410.
- Pieper R, Gatlin-Bunai CL, Mongodin EF, Parmar PP, Huang ST, Clark DJ, Fleischmann RD, Gill SR, Peterson SN (2006) Comparative proteomic analysis of Staphylococcus aureus strains with differences in resistance to the cell wall-targeting antibiotic vancomycin. Proteomics. 6(15): 4246–4258.
- Polak J, Della Latta P, Blackburn P (1993) In vitro activity of recombinant lysostaphin-antibiotic combinations toward methicillin-resistant Staphylococcus aureus. Diagn Microbiol Infect Dis. 17: 265–270.
- Ramadurai L, Jayaswal RK (1997) Molecular cloning, sequencing, and expression of lytM, a unique autolytic gene of Staphylococcus aureus. J Bacteriol. 179(11): 3625–3631.
- Rogers KL, Fey PD, Rupp ME (2009) Coagulase-negative staphylococcal infections. Infect Dis Clin N Am. 23: 73–98.
- Rohrer S, Berger-Bächi B (2003) FemABX peptidyl transferases: a link between branched-chain cell wall peptide formation and β-lactam resistance in Gram-positive cocci. Antimicrob Agents Chemother. 47: 837–846.
- Schudhardt VT, Schindler CA (1964) Lysostaphin therapy in mice infected with Staphylococcus aureus. J Bacteriol. 88: 815–816.
- Shah A, Mond J, Walsh S (2004) Lysostaphin-coated catheters eradicate Staphylococcus aureus challenge and block surface colonization. Antimicrob Agents Chemother. 48: 2704–2707.
- Sharif S, Singh M, Kim SJ, and Schaefer J (2009) Staphylococcus aureus Peptidoglycan Tertiary Structure from Carbon-13 Spin Diffusion. J Am Chem Soc. 131(20): 7023–7030.
- Simmonds RS, Simpson WJ, Tagg JR (1997) Cloning and sequence analysis of zooA, a Streptococcus zooepidemicus gene encoding a bacteriocin-like inhibitory substance having a domain structure similar to that of lysostaphin. Gene. 189: 255–261.
- Singh VK, Carlos MR, Singh K (2010) Physiological significance of the peptidoglycan hydrolase, LytM, in Staphylococcus aureus. FEMS Microbiol Lett. 311(2): 167–175.
- Smith TJ, Blackman SA, and Foster SJ (2000) Autolysins of Bacillus subtilis: multiple enzymes with multiple functions. Microbiology. 146: 249–262.
- Strandén AM, Ehlert K, Labischinski H, Berger-Bächi B (1997) Cell wall monoglycine crossbridges and methicillin hypersusceptibility in a femAB null mutant of methicillin-resistant Staphylococcus aureus. J Bacteriol. 179: 9–16.
- Sugai M, Fujiwara T, Akiyama T, Ohara M, Komatsuzawa H, Inoue S, and Suginaka H (1997) Purification and molecular characterization of glycylglycine endopeptidase produced by Staphylococcus capitis EPK1. J Bacteriol. 179: 1193-1202.
- Tamura A, Ohashi N, Urakami H & Miyamura S (1995) Classification of Rickettsia tsutsugamushi in a new genus, Orientia gen. nov., as Orientia tsutsugamushi comb. nov. Int J Syst Bacteriol. 45: 589–591.
- Thumm G, Götz F (1997) Studies on prolysostaphin processing and characterization of the lysostaphin immunity factor (Lif) of Staphylococcus simulans biovar staphylolyticus. Mol Microbiol. 23: 1251–1265.
- Trayer HR, Buckley III CE (1970) Molecular properties of lysostaphin, a bacteriolytic agent specific for Staphylococcus aureus. J Biol Chem. 245: 4842–4846.
- van Heijenoort (2001) Formation of the glycan chains in the synthesis of bacterial peptidoglycan. J Glycobiology. 11:25R–36R.
- Vollmer W, and Tomasz A (2000) The pgdA gene encodes for a peptidoglycan N-acetylglucosamine deacetylase in Streptococcus pneumonia. J Biol Chem. 275: 20496–20501.
- Vollmer W, Blanot D and De Pedro MA (2008) Peptidoglycan structure and architecture. FEMS Microbiology Reviews. 32(2): 149–167.
- Walsh S, Shah A, Mood J (2002) Improved pharmacokinetics and reduced antibody reactivity of lysostaphin conjugated to polyethylene glycol. Antimicrob Agents Chemother. 47: 554–558.
- Williamson CM, Bramley AJ, Lax AJ (1994) Expression of the lysostaphin gene of Staphylococcus simulans in a eukaryotic system. Appl Environ Microbiol. 60: 771–776.
- Wretlind B, Hedén L, Wadström T (1973) Formation of extracellular haemolysin by Aeromonas hydrophila in relation to protease and staphylolytic enzyme. J Gen Microbiol. 78(1): 57-65.
- Wu JA, Kusuma C, Mond JJ, Kokai-Kun JF (2003) Lysostaphin disrupts Staphylococcus aureus and Staphylococcus epidermidis biofilms on artificial surfaces. Antimicrob Agents Chemother. 47: 3407–3414.
- Xia G and Peschel A (2008) Toward the Pathway of S. aureus WTA Biosynthesis. Chem Biol.


